パーキンソン病は、世界で最も多い運動症状を呈する脳の病気であり、進行を抑制する根本的な治療法がまだ見つかっていない神経難病です。
今回、東京大学大学院医学系研究科神経内科学の戸田達史教授と、神戸大学大学院医学研究科神経内科学の上中健医師らの研究グループは、悪性黒色腫(注1)に対する薬として承認されているダブラフェニブが、パーキンソン病の進行を抑制する可能性を持つことを見出しました。
戸田教授らは、大阪大学の岡田随象教授が開発した薬剤データベースなどを利用した解析を用いて、パーキンソン病の治療薬候補を同定しました。そのうちの1つであるダブラフェニブが、培養細胞やマウスのパーキンソン病モデルにおいて実際に神経保護効果を示すことを世界で初めて証明しました。この成果により、パーキンソン病の進行を抑制する研究が進むことが期待されます。また、この薬剤スクリーニング手法は、アルツハイマー病や筋萎縮性側索硬化症などの他の神経難病のみならず、糖尿病や高血圧症といった様々な疾患で有用な可能性があります。
この研究成果は、8月16日(日本時間)に英国科学誌「Human Molecular Genetics」にオンライン掲載されました。
ポイント
- パーキンソン病は、世界で最も多い運動症状を呈する神経変性疾患であり、進行を抑制する根本的な治療法がまだ見つかっていない難病であるが、薬剤データベースなどを利用した解析により、パーキンソン病の治療薬候補を同定した。
- そのうちの1つである、悪性黒色腫の薬として既に承認されているダブラフェニブが、培養細胞やマウスのパーキンソン病モデルにおいて実際に神経保護効果を示すことを世界で初めて証明した。
- パーキンソン病の進行を止める薬は存在しないため、臨床応用できるようになればその意義は大きい。今後は最も適切な投与量・投与法の研究をすすめる。この薬剤スクリーニング手法は、アルツハイマー病や筋萎縮性側索硬化症などの他の神経変性疾患のみならず、糖尿病や高血圧症といった遺伝的要因の関与が考えられる様々な疾患で有用な可能性がある。
研究背景
パーキンソン病は脳のドパミン神経細胞が減少するために、手足の震えや歩行障害などの運動症状を呈する進行性の神経難病です。65歳以上の1~2%に発症するとされており、症状を緩和する対症療法薬は複数存在しますが、病気の進行を抑制する根本的な治療薬は未だ見つかっていません。
薬剤をゼロから開発して臨床試験をクリアし、市場に売り出されるまでには莫大な費用と時間がかかる(1つの薬剤につき1000億円、平均15年)とされています。そのためシルデナフィルなどのように、既に特定の疾患で承認されている薬剤の中から新たに別疾患に使える薬を見出す「drug repurposing」という手法が、開発期間やコストの短縮に繋がるため注目されています。
パーキンソン病の大部分は孤発性(注2)の発症形式をとり、神戸大学も含めた複数の施設においてゲノムワイド関連解析(Genome-Wide Association Study:GWAS)(注3)により発症に関連する遺伝子が同定されてきましたが、こういった知見をどうすれば疾患の治療につなげられるかという課題が今まで残されていました。
研究内容
戸田達史教授らは、2014年に現大阪大学遺伝統計学の岡田随象教授らが関節リウマチにおいて開発した薬剤スクリーニングの手法に着目しました。これは、ゲノムワイド関連解析の結果と、薬剤データベースやタンパク質間相互作用のデータベースを活用し、drug repurposingを含めた新規治療薬の同定を行う方法です。孤発性パーキンソン病において同様の解析を行い、57種類の他疾患で承認されている薬剤をパーキンソン病の治療薬候補として同定しました。
同定された候補薬剤を用いて、培養細胞やマウスに神経毒を投与したパーキンソン病モデルにおいて、実際に効果があるか検証を行いました。その結果、上記候補薬剤の中の一つであるダブラフェニブという悪性黒色腫に対する薬剤(図1)が、神経毒により誘導される細胞死を抑制することが分かりました(図2)。
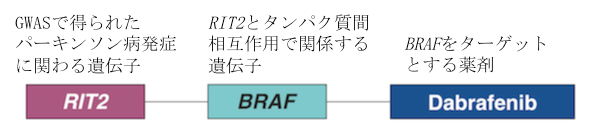
ダブラフェニブは、間接的にパーキンソン病の疾患感受性遺伝子(RIT2)をターゲットとする。
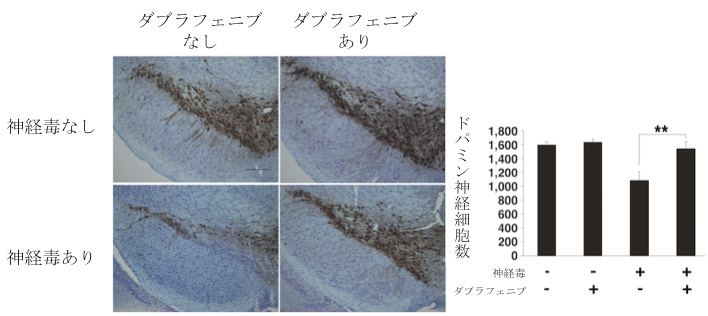
(左) マウスのドパミン神経(茶色)の免疫染色。
(右) ドパミン神経細胞数をグラフ化したもの。
神経毒投与によりドパミン神経は脱落するが、ダブラフェニブ投与により、ドパミン神経細胞死を防いだ。
今後の展望
今回の研究成果は、ダブラフェニブがパーキンソン病で見られるドパミン神経の細胞死を抑制する可能性を示しています。ダブラフェニブは悪性黒色腫において既に承認されている薬剤であるため、ヒトにおける投与量・副作用について一定のデータが存在することから、臨床応用までのコスト・期間がより少なくて済むことが期待されます。今後は、パーキンソン病の患者さんにおいて最も適切な投与量・投与方法などの研究をすすめる予定です。
また、今回用いた薬剤スクリーニングの手法は、アルツハイマー病や筋萎縮性側索硬化症などの他の神経変性疾患のみならず、糖尿病や高血圧症といった遺伝的要因の関与が考えられる様々な疾患で有用な可能性があり、今後の研究発展が期待されます。
用語解説
- (注1)悪性黒色腫
- 皮膚などに発生する悪性腫瘍。
- (注2)孤発性
- 特定の遺伝子異常に由来しないと考えられるもの。遺伝要因や環境要因が合わさって発症すると考えられている。
- (注3)ゲノムワイド関連解析(GWAS)
- その疾患の発症に関係する遺伝子を見つける代表的な方法。ヒトゲノムを網羅した数百万~1,000万の一塩基多型を用いる。特定の疾患を発症した群と健常者群とで一塩基多型の出現頻度を比較することにより、その疾患との因果関係を評価できる。
論文情報
- タイトル
- “In silico drug screening by using genome-wide association study (GWAS)-data repurposed dabrafenib, an anti-melanoma drug, for Parkinson’s disease”
- DOI
- 10.1093/hmg/ddy279
- 著者
- Takeshi Uenaka, Wataru Satake, Pei-Chieng Cha, Hideki Hayakawa, Kousuke Baba, Shiying Jiang, Kazuhiro Kobayashi, Motoi Kanagawa, Yukinori Okada, Hideki Mochizuki and Tatsushi Toda
- 掲載誌
- Human Molecular Genetics