神戸大学大学医学部附属病院 救命救急科の大野雄康 病院講師、小谷穣治 教授らの共同研究グループは、炎症性サイトカイン インターロイキン-6 (IL-6) の下流にあるシグナル分子、STAT3の特異的阻害薬により「敗血症関連骨格筋萎縮」が治療できることを世界に先駆けて見出しました。
敗血症は、感染症により過剰な炎症反応が起き、全身の臓器が障害される重篤な病態です。その合併症の一つとして、骨格筋の量や筋力が低下する「敗血症関連骨格筋萎縮」を生じることがあります。しかし、この敗血症関連骨格筋萎縮に対する有効な治療法はこれまで確立されていませんでした。今回の研究成果は、薬物療法という「敗血症関連骨格筋萎縮」への新たな治療アプローチを提案するものです。
この研究成果は、2026年1月11日に『Scientific Reports』に掲載されました。
ポイント
- 敗血症はSTAT3経路、ユビキチンプロテアソーム経路※1およびオートファジー経路の活性化を介して骨格筋萎縮を引き起こすことを示し、「敗血症関連骨格筋萎縮」の分子機構の一端を明らかにした。
- STAT3阻害薬C188-9の投与により、STAT3経路およびユビキチンプロテアソーム経路の活性が減弱し、マウスおよび筋管細胞における筋萎縮が改善することを発見した。
- 敗血症患者においても、STAT3シグナル上流の炎症性サイトカイン、IL-6血中濃度が骨格筋萎縮の重症度と関連することを見出し、STAT3阻害薬の臨床応用による新規治療の可能性を示唆した。
研究の背景
敗血症は、病原体に対する制御できない宿主の免疫反応により、多臓器不全が引き起こされた状態です。Lancet誌に掲載された2020年のデータによると、全世界で推計4,890万人の敗血症患者が発生し、しかもこの数は増え続けています。敗血症罹患患者の40-70%に、過度な炎症により「敗血症関連骨格筋萎縮」が発症します。集中治療室 (ICU) において、骨格筋萎縮が発症すると離床や人工呼吸離脱が困難になり、患者のQuality of lifeが大きく制限されます。さらに骨格筋萎縮は、長期生存率の低下とも関連しています。このような重大な問題を引き起こすにも関わらず、「敗血症関連骨格筋萎縮」の発症機序には不明点が多く、その有効な治療法もありませんでした。
研究の内容
【研究の手法】
今回、研究チームが注目したのは、代表的な炎症性サイトカインIL-6の下流にある炎症伝達シグナル、STAT3経路です。まず8-12週の雄性C57/BJ6マウスに糞便懸濁液 (1.0mg/g) を腹腔内注射し、敗血症を導入しました。治療群のマウスには敗血症導入1時間後にSTAT3阻害薬、C188-9 (50 mg/kg) を腹腔内注射しました。処置1日後、および3日後に前脛骨筋を摘出し分子細胞学的評価、および形態学的評価を行いました。さらに、細胞レベルでのより直接的な反応を観察するため、マウスC2C12筋管細胞をグラム陰性菌の細胞壁外膜を構成するリポポリサッカライド(LPS, 1 μg/mL) およびC188-9 (10μM) 存在下/非存在下で2日間培養し、同上の検討を行いました。最後に、得られた実験結果の臨床的妥当性を検証するために、神戸大学医学部附属病院ICUに入室した敗血症患者を対象とした前向き観察研究を行いました。ICU入室時のIL-6濃度と、種々の敗血症の重症度指標 (血中乳酸値、CRP、SOFA score、プロカルシトニン等) 、および腸腰筋指数 (CTで計測した腸腰筋横断面積を、身長の2乗で除した数値) の経時変化の関係を調べました。
【結果】
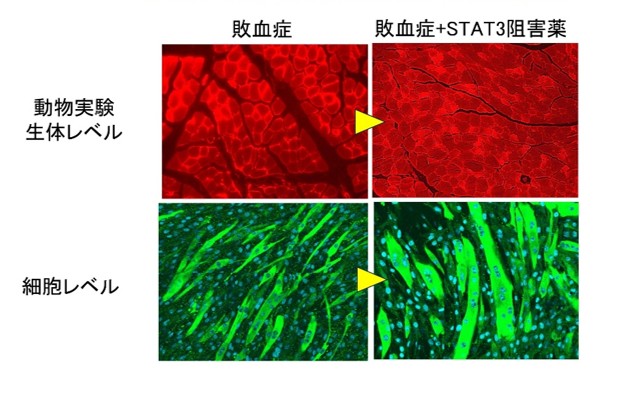
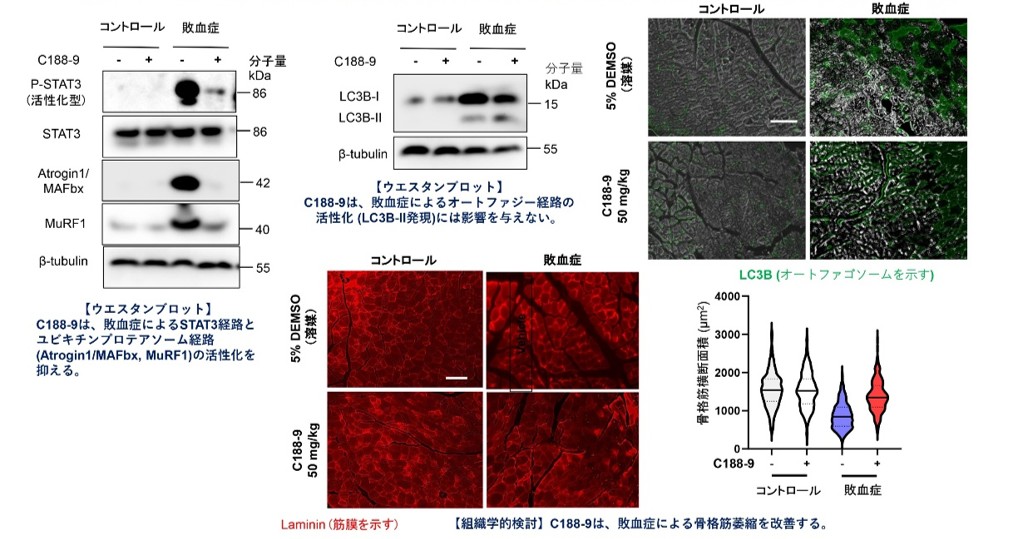
マウスにおいて、敗血症は前脛骨筋のSTAT3経路を活性化 (P-STAT3/STAT3比上昇で計測) し、さらにユビキチンプロテアソーム経路 (MuRF1およびAtrogin-1/MAFbxタンパク発現上昇) およびオートファジー経路 (LC3B-IIタンパク発現上昇と蛍光免疫染色によるLC3 dotsの増加) を活性化しました。これにより骨格筋萎縮が発症しました。C188-9投与により前脛骨筋のSTAT3経路とユビキチンプロテアソーム経路の活性が減弱し、骨格筋萎縮が改善しました。しかし、C188-9はオートファジー経路には影響を与えませんでした (図1)。
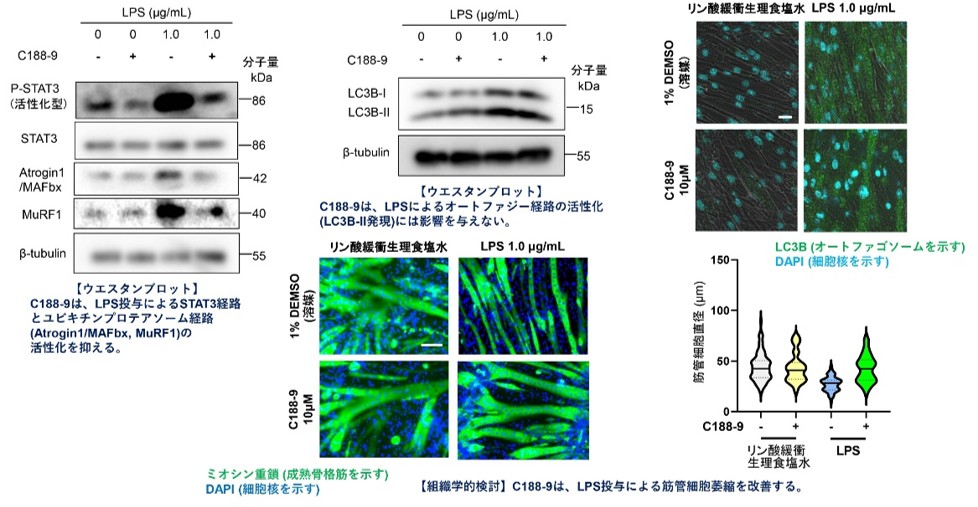
マウスC2C12筋管細胞において、LPS投与により同上のシグナルが活性化し、筋管細胞萎縮が起きました。C188-9 投与により、マウス同様STAT3経路とユビキチンプロテアソーム経路の活性が減弱し、筋管細胞萎縮が改善しました。細胞レベルでもC188-9はオートファジー経路の活性に影響を与えませんでした (図2) 。
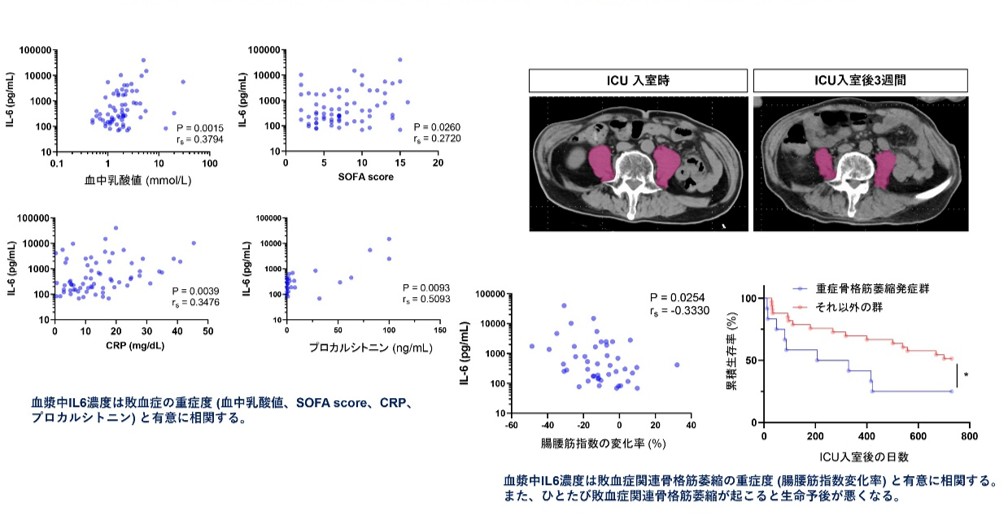
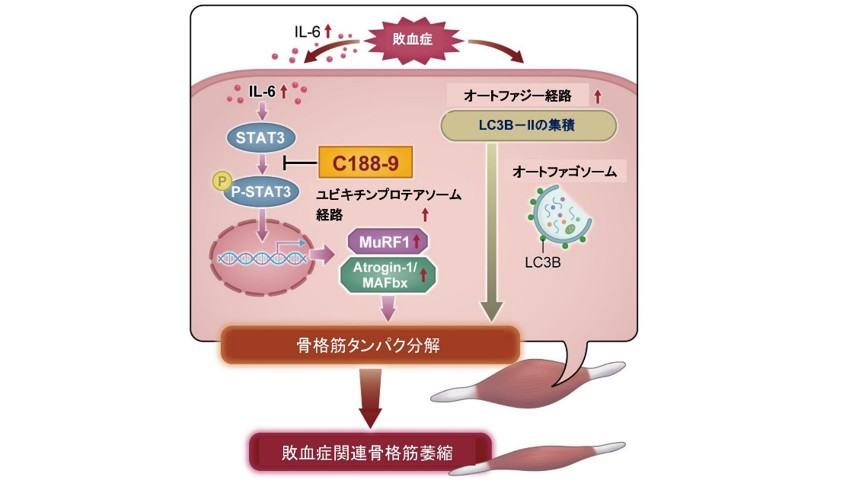
さらに敗血症患者において、血漿中IL6濃度は敗血症の重症度、および腸腰筋指数の減少率と有意に相関していました。また、敗血症関連骨格筋萎縮が重度であった群は、そうでない群に比べ累積生存率が有意に低下していました (図3)。以上の結果により、敗血症はSTAT3経路、ユビキチンプロテアソーム経路、およびオートファジー経路の活性上昇を通して骨格筋萎縮を引き起こすことが示されました (図4)。マウスおよび筋管細胞で、STAT3を薬理学的に阻害すると、ユビキチンプロテアソーム経路の活性が減弱し、「敗血症関連骨格筋萎縮」が治療できました。これらの結果は、これまで有効な治療法がなかった、「敗血症関連骨格筋萎縮」の新規治療の可能性を示唆します。
🄫 Scientific Reports(2026)(DOI: 10.1038/s41598-026-35815-9)(CC BY-NC-ND)
🄫 Scientific Reports(2026)(DOI: 10.1038/s41598-026-35815-9)(CC BY-NC-ND)
🄫Scientific Reports(2026)(DOI: 10.1038/s41598-026-35815-9)(CC BY-NC-ND)
今後の展開
STAT3経路を抑制する薬物は、重症COVID-19の治療や、関節リウマチの治療など、実臨床の現場ですでに使用されています。これらの薬物を敗血症患者に転用 (ドラッグリポジショニングといいます) することにより、「敗血症関連骨格筋萎縮」が治療でき、ひいては敗血症患者の生命予後およびQuality of lifeが改善する可能性があります。今回の研究成果は、STAT3阻害薬の臨床応用の理論的根拠を提示するものです。本研究成果に基づき、今後臨床試験が行われ、最終的には敗血症患者の生命予後、機能予後の改善につながることが期待されます。
用語解説
※1 ユビキチンプロテアソーム経路
選択性をもったタンパク分解経路。ヒトを含む哺乳類ではMuRF1およびAtrogin-1/MAFbxという2つの骨格筋特異的なユビキチンリガーゼが存在し、骨格筋タンパク分解を調整している。
謝辞
本研究は、日本学術振興会の科学研究費助成事業(JP22K09181, JP25K12250, JP21K16572, JP 24KJ1980, JP 25K12259, JP 21H03035, JP 25K10185, JP 24K19491, JP 24K12198, JP 23K08426) の支援を受けて実施されました。
論文情報
タイトル
DOI
10.1038/s41598-026-35815-9
著者
Yuko Onoa, Masafumi Saitob, Ikumi Yoshiharac, Yutaka Kondoc, Kazuho Sakamotod, Jun Sugiyamaa, Nobuto Nakanishia, Shigeaki Inouee, Joji Kotania
a: Department of Disaster and Emergency Medicine, Graduate School of Medicine, Kobe University
b: Department of Immunology and Microbiology, National Defense Medical College
c: Department of Emergency and Disaster Medicine, Graduate School of Medicine, Juntendo University
d: Department of Pharmaceutical Sciences, International University of Health and Welfare
e: Department of Emergency and Critical Care Medicine, Wakayama Medical University
掲載誌
Scientific Reports
報道問い合わせ先
神戸大学総務部広報課
E-Mail:ppr-kouhoushitsu[at]office.kobe-u.ac.jp(※ [at] を @ に変更してください)






