神戸大学大学院医学研究科内科系講座小児先端医療学(連携大学院)の飯島一誠客員教授(兵庫県立こども病院長)、神戸大学大学院医学研究科内科系講座小児科学分野の野津寛大教授及び国立成育医療研究センター佐古まゆみ部門長らを中心とする小児腎臓病研究グループは、神戸大学医学部附属病院 臨床研究推進センターを試験調整事務局として、2015年6月4日より、小児期発症の難治性の頻回再発型あるいはステロイド依存性のネフローゼ症候群注1,注2を対象とした多施設共同二重盲検プラセボ対照ランダム化比較試験注3を先進医療B注4として実施しました。この試験成績に基づいて、製造販売業者である中外製薬株式会社が免疫抑制剤「セルセプト® カプセル250、セルセプト®懸濁用散31.8% 」[一般名:ミコフェノール酸モフェチル]において、難治性のネフローゼ症候群(頻回再発型あるいはステロイド依存性を示す場合)に対する適応追加の承認を2025年9月19日付で厚生労働省より取得しました。今回、日本で、難治性の頻回再発型/ステロイド依存性ネフローゼ症候群に対するリツキシマブ投与後の寛解維持療法としての適応を取得したのは、世界で初めてのことです。今後、難治性の頻回再発型/ステロイド依存性ネフローゼ症候群に対するリツキシマブ投与後の再発が抑制され、患者さんのQOLの向上が期待されます。
研究の背景
小児ネフローゼ症候群は小児の慢性腎疾患で最も頻度が高く、日本では、小児人口10万人あたり年間6.49人(全国で約1,000人)の小児が、この病気を発症します。尿中に大量のタンパク質が漏れ出て血液中のタンパク質が極端に少なくなる原因不明の難病で、小児慢性特定疾病及び指定難病に指定されています。小児ネフローゼ症候群の80-90%はステロイドに反応し寛解となるステロイド感受性ネフローゼ症候群注5ですが、その半数はステロイドの減量・中止により頻回に再発するためステロイドを長期継続投与せざるを得ず、ステロイドの副作用を軽減するために様々な免疫抑制薬が用いられステロイドの減量・中止が試みられます。しかし、全体の約20%の患者は、免疫抑制薬を用いてもステロイドを中止できない“難治性頻回再発型/ステロイド依存性ネフローゼ症候群”となるために、新たな治療法の開発が望まれていました。
小児腎臓病研究グループ参加施設の9施設において2008年より医師主導治験注6として実施された難治性頻回再発型/ステロイド依存性ネフローゼ症候群に対するリツキシマブ(Bリンパ球表面抗原CD20に対するモノクローナル抗体)の多施設共同二重盲検プラセボ対照ランダム化比較試験により、その有効性・安全性が検討され(Iijima K et al. Lancet 2014)、その結果等をもとに2014年8月29日付で適応拡大が承認され保険診療が可能となりました。
しかし、同時に大半の症例でリツキシマブによって枯渇した末梢血Bリンパ球が次第に回復するのに伴い、頻回再発/ステロイド依存性再発をきたすことも明らかになり、リツキシマブ投与後の寛解維持療法の開発が強く望まれていました。
日本で実施されたパイロット研究(Ito S et al. Pediatr Nephrol 2011)で、リツキシマブ投与後に免疫抑制薬のひとつであるミコフェノール酸モフェチル(MMF)を投与することで寛解維持期間を延ばすことができることが示唆されたこともあり、小児腎臓病研究グループは、MMFがリツキシマブ投与後の寛解維持療法として有効かつ安全であるか否かを検討する多施設共同二重盲検プラセボ対照ランダム化比較試験を先進医療Bの枠組みの中で実施しました。
研究の内容
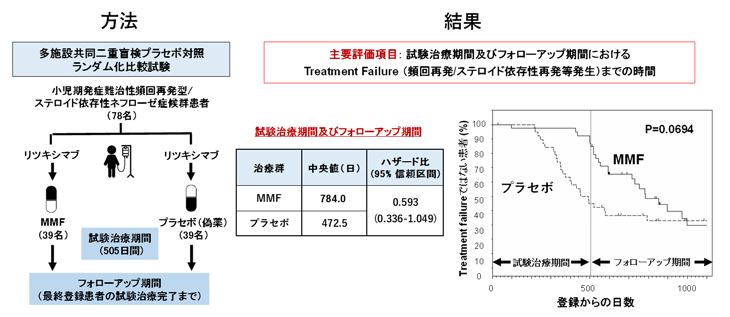
本研究では、小児期発症難治性頻回再発型/ステロイド依存性ネフローゼ症候群患者に対して、リツキシマブ375 mg/m2/回(最大投与量 500 mg/回)を1週間間隔で計4回静注投与した後に、寛解維持療法としてMMF(39例)もしくはプラセボ(39例)の1,000~1,200 mg/m2/日(最大投与量 2 g/日)(1日2回)を17か月間(505日まで)経口投与し、その後、フォローアップ期間として再発を認めるまで可能な限り無治療で経過観察を行いました。
主要評価項目である試験治療期間及びフォローアップ期間を通じてのtreatment failure(頻回再発、ステロイド依存性再発あるいはステロイド抵抗性再発)となるまでの期間は、統計学的には有意ではないもののMMF群では長い傾向にあり(中央値:784.0 vs. 472.5日, P=0.0694)、MMF群のプラセボ群に対するハザード比注7は0.593 (95%信頼区間注8:0.336-1.049)と、treatment failureの発生を41%抑制しました。本試験では、副次評価項目である試験治療期間中の再発回数は、MMF群ではプラセボ群に比して少なく、試験治療期間中のステロイド投与量も減少させる傾向がみられました。安全性に関しては両群間に大きな違いは認めませんでした。以上より、MMFはリツキシマブ投与後の寛解維持療法として有効であり、安全性も許容範囲内であると考えられました。(詳細は、2021年12月2日付けプレスリリースを参照。)
2022年10月18日、日本小児腎臓病学会は、難治性のネフローゼ症候群(頻回再発型あるいはステロイド依存性を示す場合)に対するリツキシマブ治療後の寛解維持療法としてのミコフェノール酸モフェチルに関して厚生労働省に未承認薬・適応外薬の要望(募集対象(3))を提出、2025年3月6日の薬事審議会第一部会で、医療上の必要性の高い未承認薬・適応外薬検討会議注9の報告書に基づき、公知申請注10を行っても差し支えないとされ、その後、中外製薬株式会社により公知申請が行われ、2025年9月19日付で適応追加の承認を取得しました。
この研究の意義と今後の展開
ミコフェノール酸モフェチルは、ネフローゼ症候群に対して、世界的に、しばしば用いられている薬剤ですが、いずれの国でも適応外使用されています。今回、日本で、難治性の頻回再発型/ステロイド依存性ネフローゼ症候群に対するリツキシマブ投与後の寛解維持療法としての適応を取得したのは、世界で初めてのことです。日本でミコフェノール酸モフェチルの使用が承認されたことで、日本における難治性の頻回再発型/ステロイド依存性ネフローゼ症候群に対するリツキシマブ投与後の再発が抑制され、患者さんのQOLの向上が期待でき、その意義は大きいと考えられます。
用語解説
注1.ネフローゼ症候群
ネフローゼ症候群とは、尿にタンパク質がたくさん出てしまうために、血液中のタンパク質が減り(低タンパク血症)、その結果、むくみ(浮腫)が起こる疾患である。明らかな原因がわからないものを、一次ネフローゼ症候群と呼ぶ。国の指定難病及び小児慢性特定疾病の一つ。
注2.難治性頻回再発型/ステロイド依存性ネフローゼ症候群
免疫抑制薬等の治療によっても頻回再発やステロイド依存性再発を生じ、ステロイドの長期投与をせざるを得ない病態のこと。
注3.多施設共同二重盲検プラセボ対照ランダム化比較試験
二重盲検比較試験とは、実施する側(医療従事者)と患者が、投与される薬がプラセボか実薬かを判別できない形で実施される比較試験のことで、プラセボ対照ランダム化比較試験は、被験者を無作為に、実薬を投与するグループとプラセボを投与するグループに分け、同じ投与方法とする試験デザインである。両者を組み合わせ、また、必要な患者数を確保するために多施設共同として実施される多施設共同二重盲検プラセボ対照ランダム化比較試験は、評価に主観やプラセボ効果が入ることを防ぎ、被験薬の効果や安全性を相対的に評価することが可能になり、被験薬の有効性・安全性を正確に評価できる最も標準的な手法である。
注4.先進医療B
未承認の医薬品や医療機器を用いても、一定の条件を満たせば保険診療との併用を可能としたもの。未承認の医薬品等の使用を伴わない先進医療Aと、未承認の医薬品等の使用を伴う先進医療Bに大きく分類されている。
注5.ステロイド感受性ネフローゼ症候群
ネフローゼ症候群のうち、ステロイド連日投与開始後4週間以内に完全寛解する(症状が治まる)もの。
注6.医師主導治験
2003年に現在の医薬品医療機器等法が改正され、それまで企業主導でしか行えなかった治験を医師が自ら企画・立案し実施することができるようになった。
注7.ハザード比
統計学上の用語で、臨床試験などで使用する相対的な危険度を客観的に比較する方法。例えばA薬と対照のB薬を比較するという臨床試験でハザード比が0.60という結果であれば、A薬はB薬よりリスクを40%減少させたという意味になる。
注8.95%信頼区間
母集団の統計量(真の値)が95%の確率で収まる値の範囲のこと。一般には、比の検定ではこの範囲が1を含んでいなければ統計学的な有意差があるとされる。
注9.医療上の必要性の高い未承認薬・適応外薬検討会議
厚生労働省が設置した専門会議で、国内で未承認または適応外とされている薬剤のうち、患者の治療に不可欠と認められるものについて、導入の可否を検討する場。
注10.公知申請
海外では承認されているが日本では未承認のため使用できない医薬品等について、有効性や安全性など科学的根拠が十分と認められた場合には医学薬学上「公知」であるとされ、臨床試験の一部あるいは全部を行わなくとも承認申請が可能となる制度。
報道問い合わせ先
神戸大学総務部広報課
E-Mail:ppr-kouhoushitsu[at]office.kobe-u.ac.jp(※ [at] を @ に変更してください)