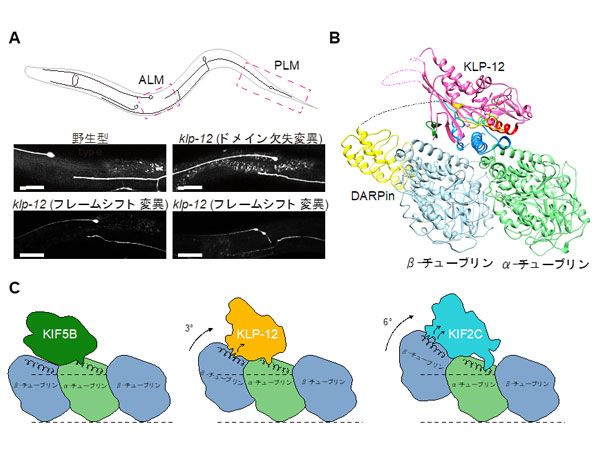
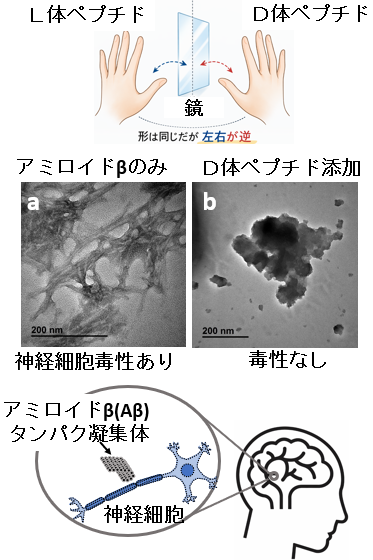
タンパク質同士がどのように選択的に結合するかは、生命現象の理解や創薬において重要な課題です。特に、特定の立体構造を持たないタンパク質を狙う分子設計は難しく、新しいアプローチが求められてきました。神戸大学大学院工学研究科の森田健太助教、丸山達生教授、近畿大学理工学部の杉本邦久の研究グループは、鏡像関係にある分子どうしが特異的に結合する仕組みに着目し、その原理を明らかにしました。L体とD体という鏡像関係※1にある短いペプチドが特異的に結合する「ペプチドのステレオコンプレックス形成」の仕組みを体系的に解明し、さらに、この原理を利用して設計した短いD体ペプチドが、アルツハイマー病の関連タンパク質の一つであるアミロイドβ(Aβ42)の凝集と細胞毒性を抑制することを示しました。
本研究は、これまで設計が難しかった「構造を持たないタンパク質(天然変性タンパク質)」を標的とする新しい分子設計戦略を示すもので、アルツハイマー病をはじめとする難治性疾患に対する新たな分子設計戦略につながることが期待されます。
この研究成果は、3月18日にドイツ化学会誌「Chemistry – A European Journal」でオンライン公開されました。
ポイント
- 短いL体ペプチドとD体ペプチドが特異的に結合する「ステレオコンプレックス形成」の仕組みを体系的に解明した。
- この原理を利用してアルツハイマー病関連タンパク質 Aβ42 を標的とするD体ペプチドを設計し、これがAβ42の凝集と細胞毒性を抑制することを明らかにした。
- 特定の立体構造を持たないタンパク質(IDP)を標的とする新しい分子設計手法として期待される。
研究の背景
タンパク質やペプチドは通常、L体アミノ酸から構成されています。一方で、鏡像関係にあるD体アミノ酸を含むペプチドは、生体内で分解されにくく、創薬分野で注目されています。しかし、D体ペプチドは特定のタンパク質配列と結合するのか、その設計原理はほとんど理解されていませんでした。特にアルツハイマー病の関連物質として知られるアミロイドβ(Aβ42)は、「天然変性タンパク質(Intrinsically Disordered Protein: IDP)」と呼ばれる、特定の立体構造を持たないタンパク質です。このようなタンパク質は通常の創薬戦略では標的化が難しいため、新しい分子設計の考え方が求められていました。そこで本研究では、L体ペプチドとD体ペプチドが特異的に結合して形成される「ステレオコンプレックス」に着目し、その形成条件を体系的に調べました。
研究の内容
短いペプチドの鏡像相互作用を体系的に解析
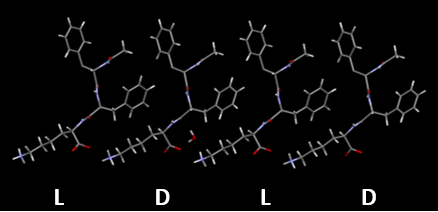
研究グループは、フェニルアラニン(F)とリシン(K)からなる三つのトリペプチド配列を設計し、L体とD体を混合したときの相互作用を調べました。その結果、FFK (L体)とffk (D体)の組み合わせが強い会合体を形成することを明らかにしました。さらに、単結晶X線構造解析により、L体とD体のペプチドが交互に並んだラセミ結晶構造を形成することが確認されました(図1)。この結合は主に次の2種類の相互作用(フェニルアラニン間の疎水性・π–π相互作用、リシンとC末端カルボキシル基の静電相互作用)によって駆動されていました。これにより、短いペプチドでも鏡像分子間で安定な会合体を形成することが示されました。
アルツハイマー病関連タンパク質を標的とするD体ペプチドを設計
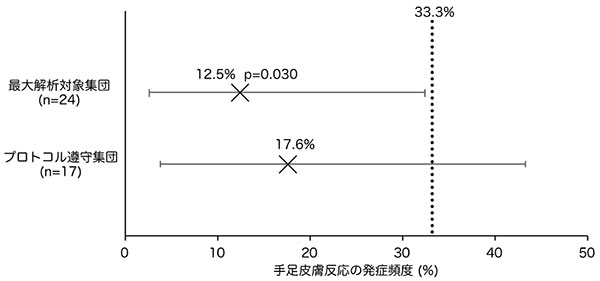
研究グループは、このステレオコンプレックス形成の原理を利用して、アルツハイマー病関連タンパク質Aβ42の配列中に存在する ペプチド配列を標的とするD体ペプチドを設計しました。その結果、設計したD体ペプチド Ac-fffakr5-NH2 は、Aβ42の線維形成(アミロイド線維)を強く抑制(図2a, b)すること、また神経細胞モデルに対する毒性を低減(図2c)することが確認されました。この効果は、Aβ42とD体ペプチドがステレオコンプレックスを形成することによって生じると考えられます。

今後の展開
本研究は、短いペプチドの鏡像相互作用の基本原理を体系的に明らかにしただけでなく、その原理を利用して天然変性タンパク質を標的とする分子を合理的に設計できることを示しました。天然変性タンパク質は、アルツハイマー病、パーキンソン病、がんなど多くの疾患に関与しています。しかし、その構造の不安定さから、これまで薬剤設計が難しいとされてきました。
今回の成果は、天然変性タンパク質を標的とする新しい創薬戦略、D体ペプチドを利用した新規治療薬開発、タンパク質機能制御分子の設計などにつながる可能性があります。本研究を基に、研究グループはアルツハイマー病治療法開発に向けて、マウス脳内でのアミロイドβ沈着抑制の研究を行っています。
用語解説
※1 鏡像関係
物体を鏡に映したときの像のように、形は同じでも左右が逆になっており、互いに完全には重ね合わせることができない関係を指す。私たちの右手と左手の関係がその典型例。化学では、このような関係にある分子を鏡像異性体(キラル分子)と呼ぶ。アミノ酸にもこの性質があり、生体のタンパク質は通常「L体」と呼ばれる形のアミノ酸で構成されているが、鏡像関係にある「D体」も存在する。
謝辞
本研究は、日本学術振興会の科学研究費助成事業(JP 23H01774、JP23K13610)、中谷財団、豊田理研スカラー、ノーリツぬくもり財団、武田科学振興財団、小柳財団、キヤノン財団、鈴木謙三記念医科学応用研究財団、AMED(24ek0109691、24ym0126808j0003)の支援を受けて実施されました。
論文情報
タイトル
"A Chirality-Guided Molecular Recognition Strategy for Targeting Intrinsically Disordered Proteins"
DOI
10.1002/chem.70889
著者
Kenta Morita,‡,[a,b] Shiho Seguchi,‡,[a] Ayaka Hayashi,[a] Haruhiko Miwa,[a] Satoru Uchida,[a] Kunihisa Sugimoto,[c] Eri Chatani,[d] Atsuo Tamura,[d] Tatsuo Maruyama*, [a,b]
[a] Department of Chemical Science and Engineering, Graduate School of Engineering, Kobe University, 1-1 Rokkodai, Nada-ku, Kobe 657-8501, Japan.
[b] Research Center for Membrane and Film Technology, Kobe University, 1-1 Rokkodai, Nada-ku, Kobe 657-8501, Japan.
[c] Graduate School of Science and Engineering, Kindai University, 3-4-1 Kowakae, Higashiosaka, Osaka 577-8502, Japan
[d] Department of Chemistry, Graduate School of Science, Kobe University, Hyogo, 657-8501, Japan
掲載誌
Chemistry – A European Journal