一重項励起子分裂はシングレット・フィッションとも呼ばれ、光照射によって生成された一分子の励起一重項状態が密集した有機色素分子同士がエネルギーを共有することで、その二分子を励起三重項状態へと変換する技術です。従来の一重項励起子分裂の応用例としては光エネルギー収支に着目した太陽光発電の高効率化が主流でしたが、一重項励起子分裂によって生み出される五重項状態と呼ばれる特殊な量子状態に着目した応用研究は未開拓でした。
今回、九州大学大学院工学研究院の川嶋優介大学院生 (当時)、濱地智之大学院生、楊井伸浩准教授、同大学大学院理学研究院の宮田潔志准教授、北里大学理学部物理学科の渡辺豪准教授の共同研究グループは、九州大学大学院工学研究院の君塚信夫教授、同大学大学院理学研究院の恩田健教授、神戸大学分子フォトサイエンス研究センターの小堀康博教授、理化学研究所開拓研究本部及び仁科加速器科学研究センターの上坂友洋主任研究員、立石健一郎研究員らと共同して、一重項励起子分裂により生じる偏極した五重項状態を用い、水分子のNMR信号強度を向上させる新たな手法の開発に成功しました。
水分子のNMRシグナルの増大は、磁気共鳴イメージング (MRI) を始めとする生体分析の分野で特に重要です。従来、一重項励起子分裂は太陽電池などエネルギー分野への応用が想定されてきましたが、本研究成果では、その量子状態を用いたNMR感度の増感というバイオ分野への新たな応用を提案しています。
本研究成果は、2023年3月1日 (日本時間) にNature Researchの国際学術誌「Nature Communications」にオンライン掲載されました。
ポイント
- 有機分子集合体で生じるエネルギー変換現象として知られる一重項励起子分裂 (シングレット・フィッション) は、これまで太陽電池などエネルギー分野への応用が想定されてきたが、その特殊な量子状態に着目した応用は未開拓だった。
- 水系溶媒中で有機色素分子の集合構造を人為的に制御することで、一重項励起子分裂によって特殊な量子状態である五重項状態を作りだし、水分子の高核偏極化 (核磁気共鳴 (NMR) 感度の増大) に初めて成功した。
- 今後、一重項励起子分裂を用いた生体分析への応用が期待される。
研究の内容と成果
分子は原子核と電子で構成されており、それぞれにスピンと呼ばれる磁石のような性質 (磁性) が備わっています。有機色素分子に光を当てて活性化した励起状態には、2つの電子スピンの向きが互いに打ち消しあった励起一重項状態と、打ち消しあっていない励起三重項状態が存在します。一重項励起子分裂とは、1つの分子の励起一重項状態から2つの分子の励起三重項状態が生成される現象です。一重項励起子分裂は一度に2つの分子に励起エネルギーを与えることができるため、光エネルギーの効率的な利用という観点から太陽電池などの分野への応用が盛んに研究されてきました。
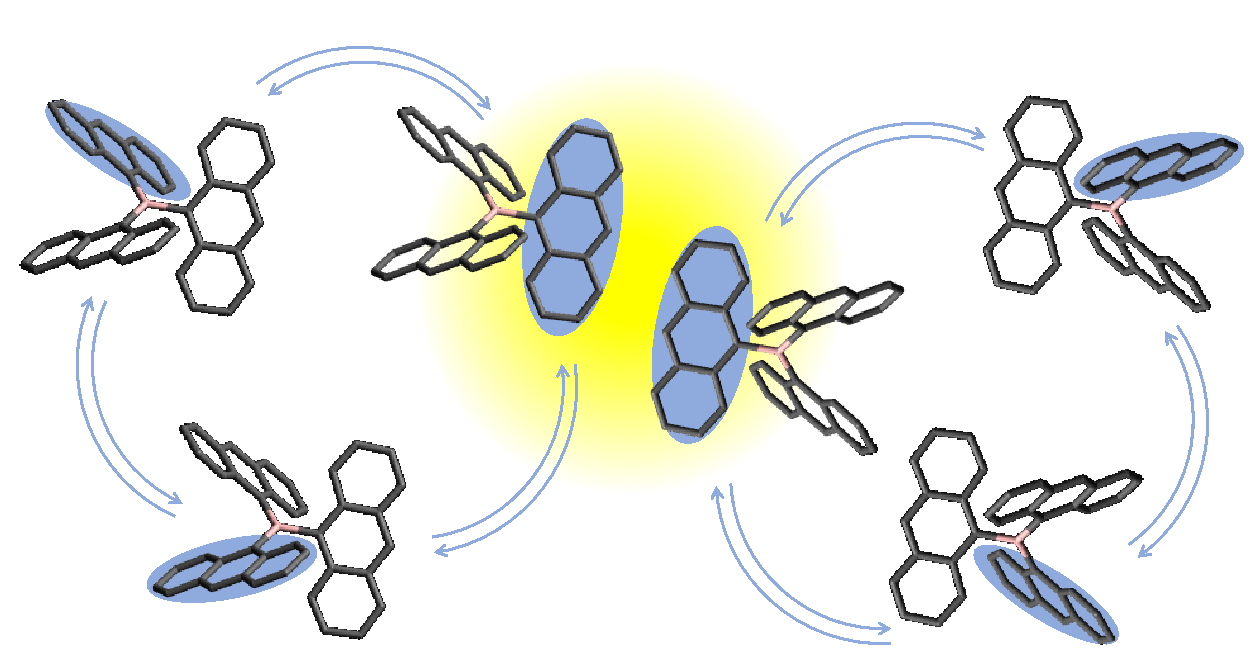
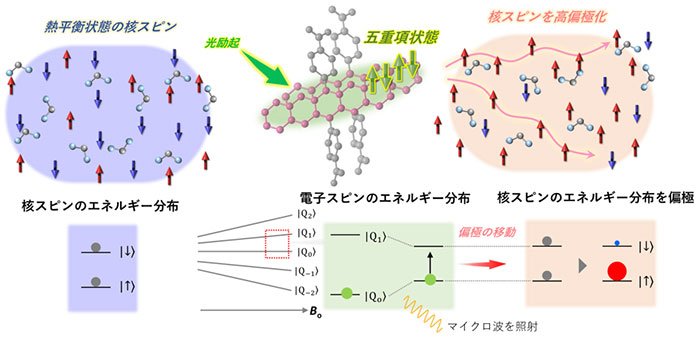
一重項励起子分裂の過程では2つの分子が励起エネルギーを共有しますが、このとき4つの電子スピンによる磁性が互いに打ち消しあわない五重項状態と呼ばれる特殊な量子状態が生み出されることが知られています (図1)。五重項状態では取りうるエネルギーの状態が5通りありますが、そのエネルギー状態の分布の度合い (偏極率) は温度によらず大きく偏っています。しかしながら、一重項励起子分裂によって生成されるこの特殊な量子状態を応用する試みは、これまで未開拓でした。
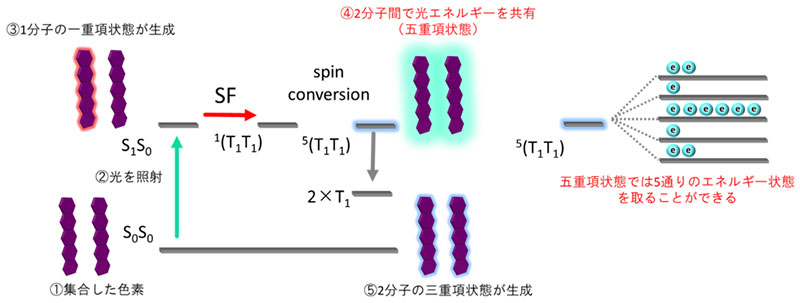
集合化している有機色素分子に光を照射すると、③のように光エネルギーを得た有機色素分子が励起一重項状態となる。励起一重項状態となった有機色素分子は周囲の分子とエネルギーを共有し、④のように2分子の間で五重項状態と呼ばれる特殊な量子状態を生成した後、⑤独立した2分子の励起三重項状態へと分かれる。五重項状態の分子のペアがとる5つのエネルギー状態のうち、特定の量子状態だけが多く生成する。
研究の内容と成果
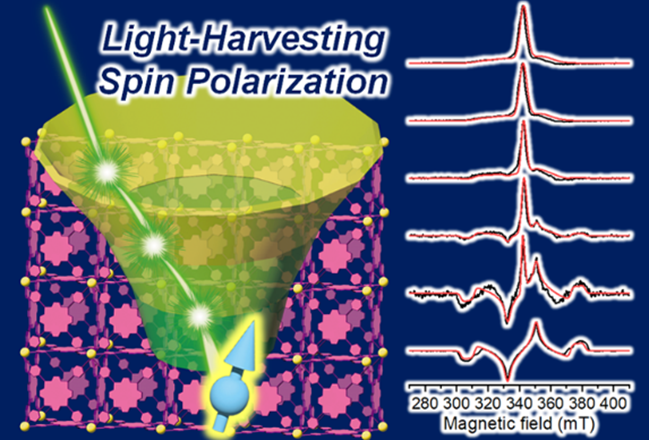
本研究グループは、一重項励起子分裂によって生成された五重項状態の電子スピンが持つ温度によらない偏極を動的核偏極法 (DNP)※1を用いて核スピンに移動することで、NMR分光法※2によるタンパク質の構造解析やMRI※3などの生体イメージングを行う場合に特に重要な水分子の高核偏極化すなわち水分子のNMR感度を、熱平衡状態と比べて20倍増大させることに成功しました。
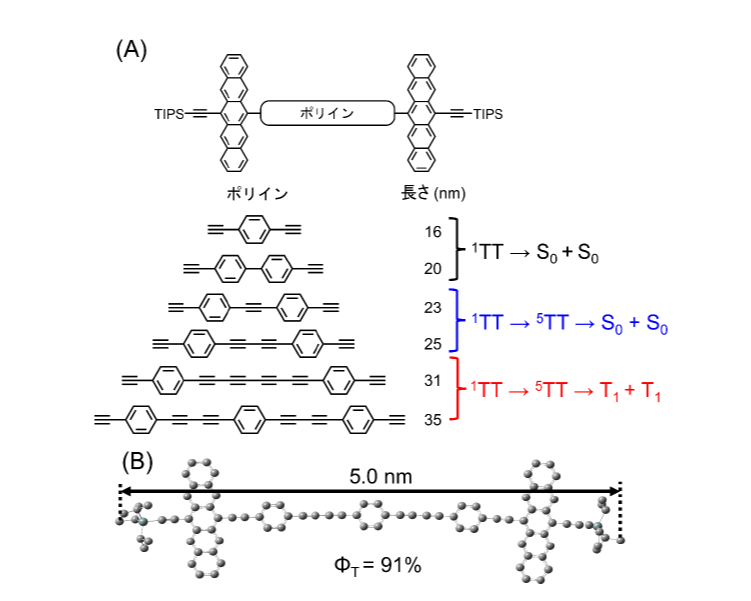
これまで一重項励起子分裂に利用される有機色素であるペンタセン誘導体は水に非常に溶けにくいことが知られていました。そこで本研究グループはこの分子に親水性の官能基を導入し、さらに内部に疎水性分子を取り込む性質を持つシクロデキストリンを導入する工夫を行いました。この結果、水系溶媒中で分子間の距離や並び方といった有機色素分子の集合構造を人為的に制御し、一重項励起子分裂特性を制御することに成功しました (図2A)。さらに、このようにして得られた有機色素分子の集合体を偏極源 (NMR増感剤) として用い、その集合体を含む溶液を急冷によってガラス化し、光照射によって五重項状態を生成させました。そしてマイクロ波を照射して一重項励起子分裂によって生成された電子スピンの偏極を利用することで、水分子のNMR感度を熱平衡状態と比べ20倍増大させることに成功しました (図2B)。また、五重項状態の電子スピン状態分布がマイクロ波との共鳴によって反転する速度であるラビ周波数が三重項状態の反転によるラビ周波数よりも大きいため、従来法よりも弱いマイクロ波強度でNMR感度の増大を行うことにも成功しています。
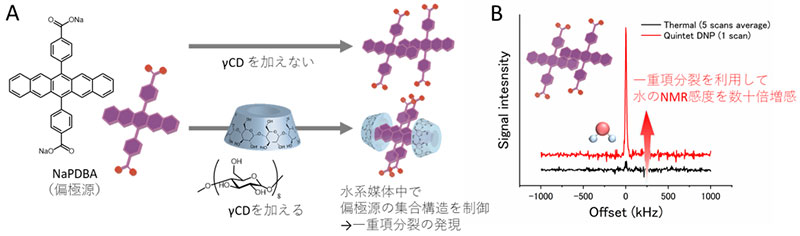
A. 本研究で用いた分子集合体。一重項励起子分裂を起こすことが知られているペンゼン環が5つ繋がったペンタセン骨格に対して親水性の部位を付与したNaPDBA (偏極源) を用いて水系溶媒中で集合化させた。この集合体に対しシクロデキストリン (γCD) を加えることでさらに集合状態を変化させ、一重項励起子分裂特性を変化させた。
B. 実際に得られたNMRスペクトル。通常のNMRスペクトル (黒線) と比較して、一重項励起子分裂により生成された五重項状態の電子スピン偏極をマイクロ波照射によって核スピンに移行したスペクトル (赤線) ではNMRシグナル強度が20倍増大した。
今後の展開
これまで一重項励起子分裂の研究分野ではバイオ系分野への応用を検討した例がありませんでした。この2つの分野を繋いだことで新たな異分野融合研究が盛んに行われることが予想されます。また水のマイクロ波の吸収が特に大きいことが、マイクロ波を用いたNMR感度の増強において従来から問題となっていました。今回の成果はマイクロ波の照射強度を抑えたまま大きな感度増強ができることを示したものであり、マイクロ波の吸収が特に大きい水中や生体でのNMR感度の向上において特に有用と思われます。今後、MRIを用いたがんの代謝イメージングに基づく診断や、NMR分光法によるタンパク質の構造や挙動のより詳細な分析に繋がることが期待されます。
用語解説
※1 動的核偏極法 (dynamic nuclear polarization: DNP)
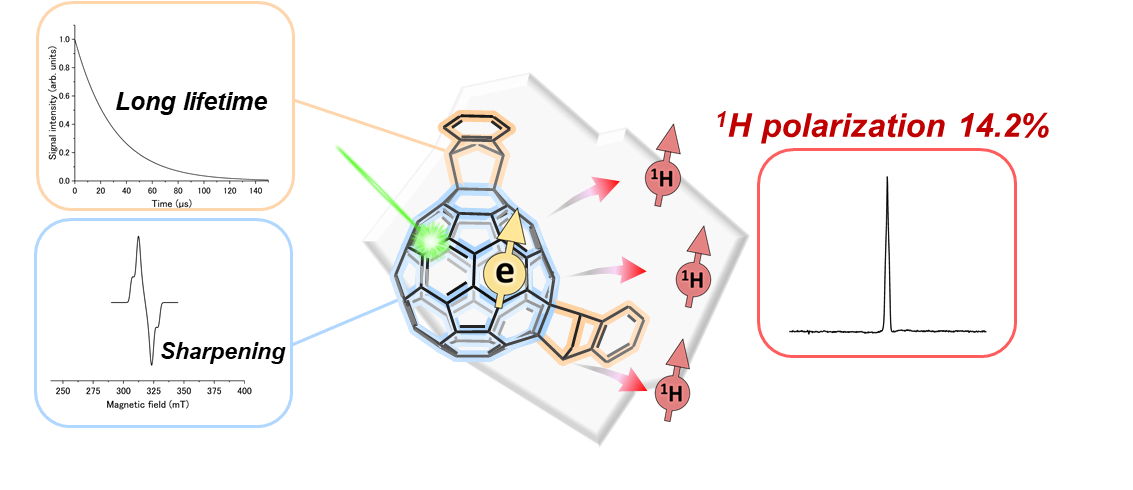
NMRの感度を増大する手法として、電子スピンの偏極を利用して核スピンの偏極を大きくする動的核偏極法 (DNP) が知られています。電子スピンのエネルギー状態の差に相当するマイクロ波を照射することで核スピンに偏極を移行することができます。電子スピンの偏極は核スピンよりも遥かに大きいため、核スピンの偏極が増大し、NMRの感度が大きく向上します (図3)。DNPで利用する電子スピンにはいくつか種類があり、ラジカル分子を利用する方法では液体ヘリウム温度以下の非常に低い温度が必要であるため装置のコストが非常に大きくなってしまいます。三重項や五重項の電子スピンは温度によらず大きな偏極を持つため、三重項状態の電子スピンを利用したTriplet-DNPが現在注目を集めていますが、マイクロ波の照射によってサンプルが加熱されてしまう点が問題視されてきました。本研究で用いた五重項状態の電子スピンを用いたDNPでは五重項状態を利用することでマイクロ波の照射強度を下げることに成功しています。
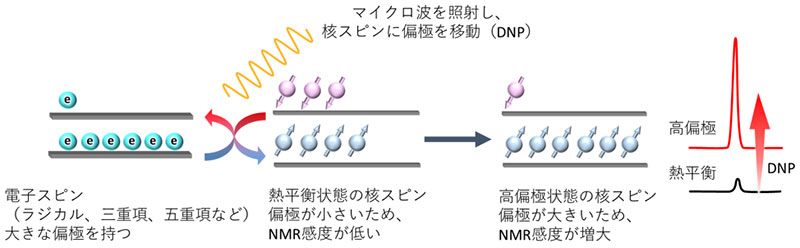
電子スピンの持つ大きな偏極をマイクロ波の照射によって核スピンに移し、核スピンの偏極を増大させることでNMRのシグナル強度を増感することが可能である。
※2 核磁気共鳴(nuclear magnetic resonance: NMR) とNMR分光法
原子核にはスピンを持つものがあり、核スピンは磁場中では磁場に対して同じ方向と逆向きの方向に分かれ、異なる2つのエネルギー状態を取ります。この2つのエネルギー状態間の共鳴現象をNMR (核磁気共鳴) と呼びます。このエネルギーの差 (共鳴周波数) は磁場に依存し、分子の置かれている環境によって核スピンの感じる磁場が異なることからNMRを用いて分子の構造や挙動を解析することができます (図4)。 このNMRの感度は核スピンの持つ2つのエネルギー状態の分布の度合い (偏極率) に依存しており、室温では分布に殆ど差が見られず、NMRの感度は非常に低いことが知られています。偏極率を大きくする手法として電子スピンの偏極を核スピンに移すDNPなどが知られていますが、従来のDNPの手法では増感に-273℃といった非常に低い温度が必要で装置コストが大きいほか、増感に強いマイクロ波の照射が必要なためサンプルが加熱されてしまうなどの問題点がありました。
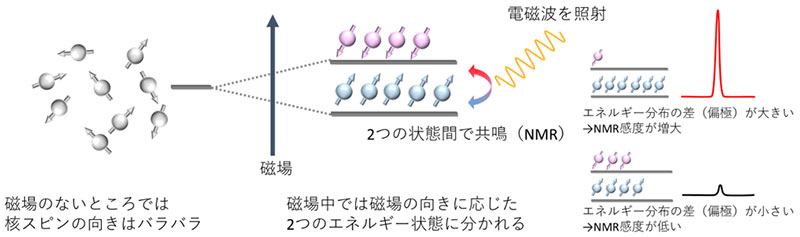
磁場中で2つのエネルギー状態に分かれた核スピンに対し、その差に相当する周波数の電磁波を照射することで共鳴が起こり、NMR信号として観測される。NMR信号の大きさは核スピンの取る2つの状態間のエネルギー分布の差 (偏極) に依存しており、その差が大きいほどNMRの感度が上昇するが、常温では10万個の核スピンのうちのわずか1つ程度の差であるため非常に感度が低い。
※3 MRI
MRIはNMRの原理を用いてサンプルの画像化を行う方法で、体内の画像化による病気の診断に利用されています。観測対象に対して位置によって異なる磁場 (勾配磁場) をかけることによって異なるNMRの共鳴周波数が得られ、NMRシグナルをマッピングした画像を作ることができます。MRIでは主に水分子のNMRシグナルを画像化していることから、水分子のNMRシグナルの増感はMRIによる生体分析を行う上で非常に重要となります。
謝辞
本研究の一部は、JST さきがけ「量子技術を適用した生命科学基盤の創出」領域 (JPMJPR18GB、研究課題名:超核偏極ナノ空間の創出に基づく高感度生体分子観測)、JST創発的研究支援事業 (JPMJFR201Y、研究課題名:MRI・NMRの未来を担う「トリプレット超核偏極の材料化学」)、日本学術振興会科学研究費 (JP17H06375、JP19H02537、JP19H05718、JP19K15508、JP20H05106、JP20H02713、JP20K21211、JP20H05676、JP19H00888、JP20H05831、JP21J13049)、JST次世代研究者挑戦的研究プログラム (JPMJSP2136) 、JST 科学技術イノベーション創出に向けた大学フェローシップ創設事業 (JPMJFS2132) 、新日本先進医療研究財団、積水化学 自然に学ぶものづくり研究助成プログラム、理研−九大科学技術ハブ共同研究プログラム、理化学研究所独創的研究課題「動的構造生物学」、九州大学エネルギー研究教育機構 (Q-PIT) のモジュール研究プログラムからの支援により行われました。
論文情報
タイトル
“Singlet fission as a polarized spin generator for dynamic nuclear polarization”
(動的核偏極法のための偏極スピン生成への一重項励起子分裂の応用)DOI
10.1038/s41467-023-36698-4
著者
川嶋優介・濵地智之・山内朗生・西村亘生・中島悠真・藤原才也・君塚信夫・笠僚宏・田村徹・西郷将生・恩田健・佐藤俊輔・小堀康博・立石健一郎・上坂友洋・渡辺豪・宮田潔志・楊井伸浩
掲載誌
Nature Communications