神戸大学大学院科学技術イノベーション研究科の蓮沼誠久教授、花王株式会社生物科学研究所、長岡技術科学大学大学院工学研究科技術科学イノベーション専攻の小笠原渉教授らの研究グループは、産業用酵素の生産菌として広く用いられる糸状菌トリコデルマ リーセイ、 (以下「トリコデルマ」) において、細胞骨格を形成するチューブリンの遺伝子破壊が、酵素生産の抑制機構として知られるカーボンカタボライト抑制※1 の緩和に繋がり、酵素生産性を大きく向上させることを発見しました。
今後、この改良を施したトリコデルマを用いることで、より安価な産業用酵素生産が可能となると期待されます。
本研究成果は、2021年2月8日にBioMed Central社のオンライン科学雑誌『Biotechnology for Biofuels』に掲載されました。
ポイント
- バイオマス糖化酵素の生産菌として知られる糸状菌トリコデルマにおいては、グルコースによって生じるカタボライト抑制が、酵素生産量・生産速度を向上させるうえでの大きな課題の一つであった。
- トリコデルマのチューブリン遺伝子を破壊することによって、グルコースによるカタボライト抑制が緩和し、酵素生産量・生産速度が大きく向上することを見出した。
- 本研究により開発された技術は、産業用酵素、特にバイオマス糖化酵素の製造技術に応用でき、バイオリファイナリーの加速に繋がると考えられる。
研究の背景
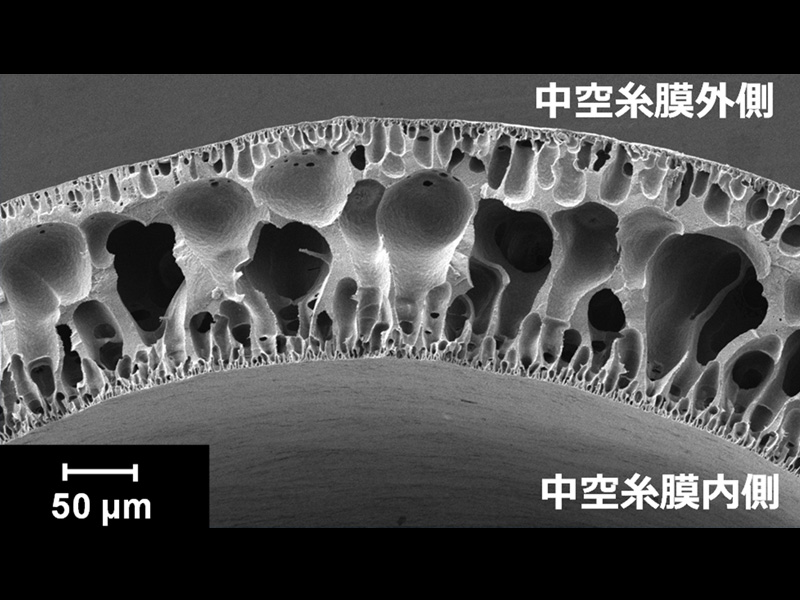
植物バイオマスは、最も世界に多く存在する資源として知られており、石油からのものづくりをオイルリファイナリーというのに対し、植物バイオマスからのものづくりはバイオリファイナリーと呼ばれています。このバイオリファイナリーを達成していくためには、バイオマスとして最も賦存量が多いセルロースを効率的に利用していくことが必要不可欠であると考えられ、このセルロースを利用しやすい糖に分解する酵素である糖化酵素は産業上とても重要です。この糖化酵素は、糸状菌トリコデルマをはじめとする微生物を培養することで生産されています。
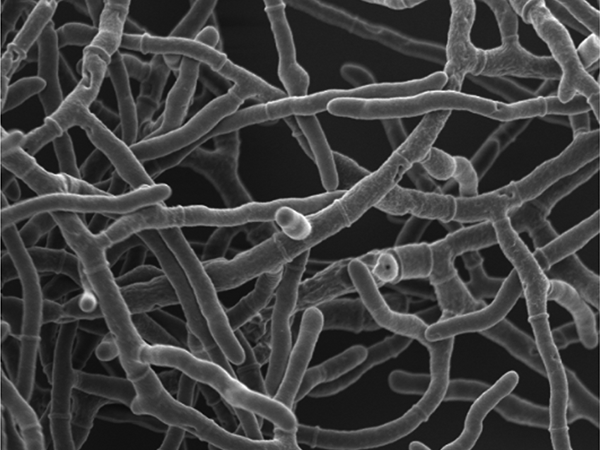
糸状菌トリコデルマ (図1) は、培養する際にセルロースを添加することで、このセルロースを分解するために糖化酵素を生産することが知られていますが、逆に分解された糖であるグルコース (ブドウ糖) が培養時に存在すると、カーボンカタボライト抑制 (炭素異化抑制) という機構により酵素の生産が抑制されることが知られています。このカーボンカタボライト抑制については、突然変異などにより解除を目指した研究が多くなされてきていますが、未だ解決には至っていませんでした。
研究の内容
研究グループではこれまでに、より効率的にセルロースを糖に分解可能な糖化酵素を生産できる遺伝子組換えトリコデルマ糸状菌の開発を進めてきましたが、その中の一つの組換え株で偶発的に酵素生産性が向上していることを見出しました。さらに、この株に生じた変異の解析を行ったところ、細胞骨格を形成するチューブリンの遺伝子が破壊されていることが明らかとなりました。
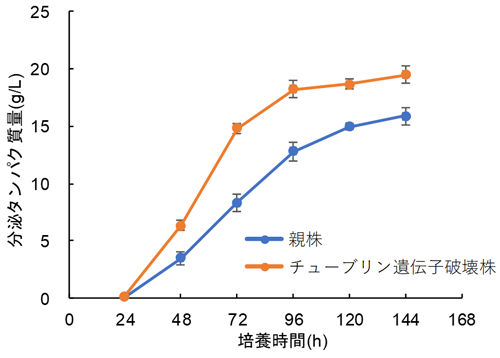
チューブリンの遺伝子破壊が酵素生産に関わる知見はこれまでに報告例がなかったため、新たにチューブリン遺伝子破壊株を構築し、破壊株の酵素生産性を評価したところ、酵素生産性が約20%、酵素生産速度が約70%向上することが明らかとなりました (図2)。さらに、この破壊株についてさまざまな条件で培養を行った結果、カーボンカタボライト抑制を引き起こすグルコースが存在する条件においても、生産性の低下が確認されず、高い酵素生産性を維持できることを見出しました。
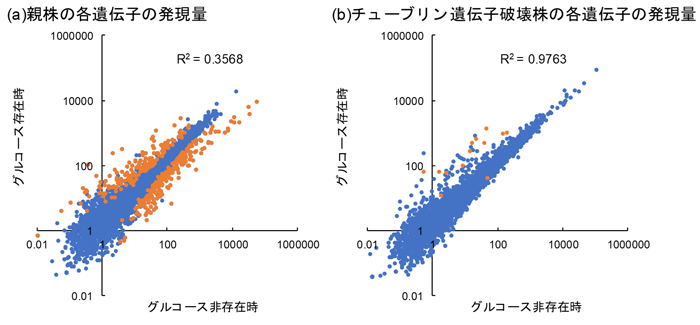
この遺伝子破壊株について、トランスクリプトーム解析※2 を実施したところ、親株においてはグルコースが培地中にあった場合に、大きく転写挙動が変化するのに対し、破壊株においてはほとんど転写挙動が変化せず、グルコースによる抑制をほとんど受けていない様子が確認されました (図3)。更に、親株と破壊株において発現変動遺伝子の解析を行ったところ、興味深いことに本来転写されていないさまざまな糖化酵素遺伝子が高発現しており、更に糖を取り込むためのタンパク質であるトランスポーターの遺伝子が高発現している様子が確認されました。
トランスポーター遺伝子が高発現していたことから、糖の取り込みについて解析を行ったところ、破壊株では、セルロースの分解産物であるセロビオースの取り込み速度が大きく向上しており、またグルコースとセロビオースが両方存在している条件においてもセロビオースを取り込むことができることが分かり、チューブリン遺伝子破壊株においては、グルコースによるカーボンカタボライト抑制が親株よりも緩和していることが明らかとなりました。
今後の展開
糸状菌トリコデルマは、産業用酵素の生産菌として産業上重要な微生物であり、本菌で酵素生産を行う上で、カーボンカタボライト抑制による生産性の低下は長年における課題となっています。今回、チューブリン遺伝子の破壊によって酵素生産性が向上し、更にカーボンカタボライト抑制の緩和が確認されたことは、本菌を用いた糖化酵素製造がより安価に実施できることに繋がり、結果的に植物バイオマスからのものづくりであるバイオリファイナリーを加速させることに繋がると考えられます。また、チューブリンがタンパク質の生産に関与していることはこれまでに報告例がなく、広く生物に保存されている遺伝子であることから、更なる作用メカニズムの解明により、より汎用的なタンパク質製造技術へと繋がっていくと考えられます。
用語解説
※1 カーボンカタボライト抑制
栄養として利用しやすい炭素源が存在する環境では利用しにくい炭素源の利用に関わる遺伝子群の発現が抑制される現象をさす。栄養として利用しやすい炭素源の代表としては、グルコース (ブドウ糖) が挙げられる。
※2 トランスクリプトーム解析
細胞内で転写されているRNAを抽出し、個々の遺伝子の転写発現量を統計学的手法により網羅的に解析する手法。DNAマイクロアレイや次世代シーケンサーを用いて行われる。
謝辞
本成果の一部は、新エネルギー・産業技術総合開発機構 (NEDO) のプロジェクト「バイオ燃料製造の有用要素技術開発事業」 (JPNP 13011) の研究助成を受けて得られました。
論文情報
タイトル
DOI
10.1186/s13068-021-01887-0
著者
Nozomu Shibata, Hiroshi Kakeshita, Kazuaki Igarashi, Yasushi Takimura, Yosuke Shida, Wataru Ogasawara, Tohru Koda, Tomohisa Hasunuma* & Akihiko Kondo
- * Corresponding author
掲載誌
Biotechnology for Biofuels