埼玉県立小児医療センター 岡明病院長、日本大学医学部附属板橋病院小児科・新生児科 森岡一朗教授、神戸大学医学部附属病院小児科 野津寛大教授、東京大学医学部附属病院小児・新生児集中治療部 高橋尚人教授らの研究グループは、2020年2月1日より、症候性先天性サイトメガロウイルス (CMV)※1 感染児を対象としたバルガンシクロビル塩酸塩ドライシロップの有効性および安全性を評価する多施設共同医師主導治験を実施し、今般、良好な成績を得ました。
この研究成果は2022年6月21日にJournal of Clinical Medicineに掲載されました。
この結果は、バルガンシクロビル塩酸塩ドライシロップが希少疾患である症候性先天性CMV感染症に苦しむ患者さんの治療の新たな選択肢となることを示しており、患者さんにより良い治療を提供できる可能性があります。
なお、本治験は、日本医療研究開発機構 (AMED)「成育疾患克服等総合研究事業—BIRTHDAY」(研究開発課題名:症候性先天性サイトメガロウイルス感染症を対象としたバルガンシクロビル治療の開発研究) の支援を受けて実施されました。
ポイント
- 症候性先天性CMV感染症は、聴覚障害、発達遅延等の重い後遺症を残す可能性がある最も頻度の高い先天性感染症であり、患者本人のみならず保護者にも大きな疾病負荷となる。
- 国内外で症候性先天性CMV感染症の適応を持つ治療薬はなく、その開発が熱望されている。
- 今回、症候性先天性CMV感染症に対して、バルガンシクロビルの有効性及び安全性を評価する医師主導治験が実施され、良好な成績が確認された。
- 本試験で示された結果は、バルガンシクロビルが当該疾患の治療選択肢になることを示しており、この疾病に苦しむ患者に、より良い治療が提供できる可能性がある。
先天性サイトメガロウイルス感染症について
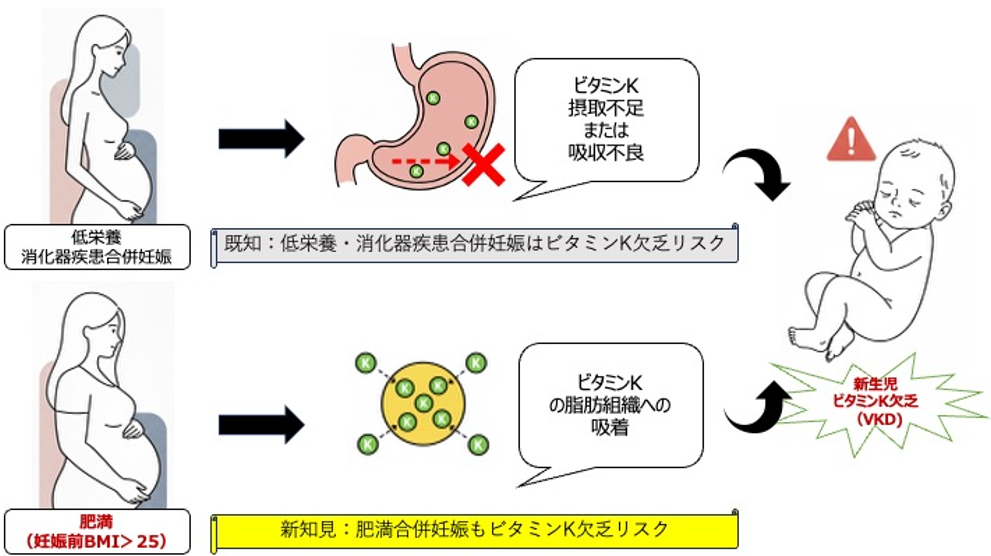
先天性サイトメガロウイルス (CMV) 感染症は、CMVの母子感染※2によって、聴覚障害、発達遅延等の重い後遺症を残す可能性がある最も頻度の高い先天性感染症です。我が国の年間総出生児の0.3% (約2700人/90万人出生) が先天性CMV感染で出生しています。その感染児の約20%が、出生時に何らかの臨床症状を有して出生する症候性先天性CMV感染症です。この症候性先天性CMV感染症の約80%が、その後の乳幼児期に難聴や発達遅延を生じており、我が国の小児に大きな疾病負荷を与えています。
CMVに対する代表的な治療薬として、経口で投与可能なバルガンシクロビル※3が存在しますが、症候性先天性CMV感染症が重い後遺症を残す可能性があるにもかかわらず、世界中で保険適用がありません。
バルガンシクロビルの有効性および安全性を評価する医師主導治験
抗CMV薬であるバルガンシクロビルを生後早期から投与することにより、聴力障害や発達遅延の治療、または症状進展を抑制しうることが、我が国や諸外国の臨床研究で示されています。我が国では、生後3週以内の新生児尿を用いた先天性CMV感染の診断が一般診療で可能となっていることから、本薬の保険承認下での使用が熱望されています。
本治験では、後障害を引き起こす可能性の高い中枢神経障害を呈する症候性先天性CMV感染症を対象とし、バルガンシクロビル経口液剤(バルガンシクロビル塩酸塩ドライシロップ)治療の第III相多施設共同非盲検単群医師主導試験※4, ※5を実施しました。
研究の内容と結果
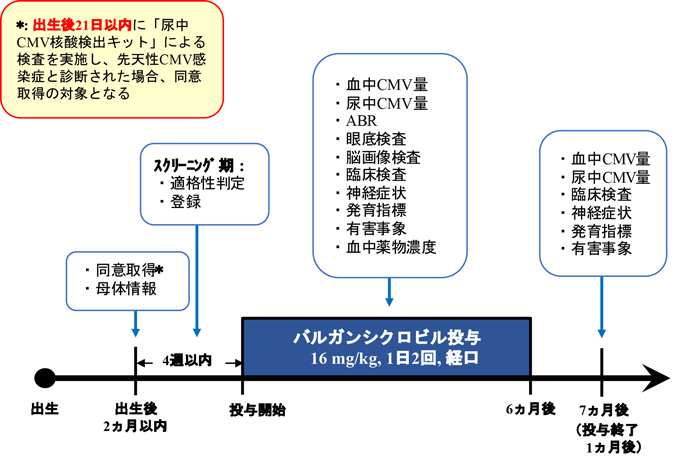
本研究グループでは、中枢神経障害を呈する症候性先天性CMV感染児を対象として、バルガンシクロビルの有効性および安全性を評価する医師主導治験を実施しました。全国6つの大学病院において、被験者の代諾者から文書により同意を取得した25名を対象とし、うち24名に対してバルガンシクロビルを1回16mg/kg、1日2回、6ヵ月間経口投与しました。投与6ヵ月時点における全血中のCMV量 (ウイルス量) の治療前からの変化、並びに聴力障害の程度の変化を評価しました。
その結果、全血中CMV量 (ウイルス量) は治療前と比較して統計学的に有意な減少が認められました (変化量[中央値]:−246.0 IU/mL,p<0.0001)。また、聴力障害の程度 (Best ear assessment) ※6は改善 (24名中14名,58.3%) または不変であり、悪化した症例はありませんでした。
この研究の意義と今後の展開
これまでに症候性先天性CMV感染症に対する海外での研究結果は報告されていましたが、治験の厳格な基準に基づいて有効性及び安全性を評価したのは今回が初めてです。
出生後に早期に治療介入することで、CMV量を減少させることができ、難聴や精神運動発達遅延の改善あるいは進展回避により、患者の社会的予後の改善に大きな影響を及ぼすことが期待でき、その意義は大きいと考えられます。
今回の治験結果に基づき、症候性先天性CMV感染症の患者さんが正式な保険診療として本剤を使用できるようにするため、バルガンシクロビルドライシロップの追加の適応症として症候性先天性CMV感染症を関係当局に申請中です。
用語の説明
- ※1 サイトメガロウイルス
- 正式名称はヒトヘルペスウイルス5 (HHV-5) で、様々な細胞・組織に感染することができる。一般に、健常な小児や成人は、CMVに感染しても症状を呈することは少ない。しかし、免疫抑制状態である移植を受けた患者や後天性免疫不全症候群 (エイズ) の患者、母子 (先天性) 感染では、重篤な病気を発症することが知られている。
- ※2 母子感染および母子感染症
- 細菌やウイルスなどの何らかの病原微生物がお母さんから赤ちゃんに感染することを「母子感染」という。サイトメガロウイルスは、赤ちゃんがお腹の中で感染する胎内感染を引き起こすことがある。母子感染の結果、病気を発症することを「母子感染症または先天性感染症」という。
- ※3 バルガンシクロビル
- バルガンシクロビルは、抗サイトメガロウイルス薬の1つ。ウイルスの複製を阻害することにより、抗ウイルス効果を発揮する。静脈内投与を必要とするガンシクロビルをL-バリンでエステル化したプロドラッグであり、経口投与ができる。小児用製剤であるバルガンシクロビルの経口液剤 (バルガンシクロビル塩酸塩ドライシロップ) が、2018年12月より我が国でも使用可能である。我が国の適応疾患は、後天性免疫不全症候群 (エイズ)・臓器移植 (造血幹細胞移植も含む)・悪性腫瘍におけるサイトメガロウイルス感染症と臓器移植 (造血幹細胞移植を除く) におけるサイトメガロウイルス感染症の発症抑制である。注意すべき副作用として、骨髄抑制 (特に好中球減少)、動物実験で催奇形性、精子形成の低下、発癌性がある。
- ※4 第III相多施設共同非盲検単群試験
- 多くの患児 (本治験では25人) について、「くすり」の有効性、安全性、使い方を最終的に確認した (第III相試験)。確認の方法は、一般にはプラセボ (偽薬) を用いて治療者や被験者ともに分からないようにして比較を行うが、本治験では実薬のみを用いて中身を明らかにした非盲検単群試験で行った。また、本治験は、6施設 (東京大学病院、日本大学板橋病院、名古屋大学病院、藤田医科大学病院、神戸大学病院、長崎大学病院) での共同試験として実施した。
- ※5 医師主導治験
- 治験の準備から管理を医師自ら行うことを医師主導治験という。医師主導治験では、治療薬が必要とされているにも関わらず、採算性の問題等で製薬会社が治験を実施できない薬や既に承認されている薬の適応症を拡大することなどを目的に医師が自ら治験の計画を立てて治験を実施する。
- ※6 Best ear assessment
- 各被験者の両耳 (右耳,左耳) のうち成績の良い方の評価を採用すること。
論文情報
- タイトル
- “Oral Valganciclovir Therapy in Infants Aged ≤2 Months with Congenital Cytomegalovirus Disease: A Multicenter, Single-Arm, Open-Label Clinical Trial in Japan”
- DOI
- 10.3390/jcm11133582
- 著者
- Ichiro Morioka, Yasumasa Kakei, Takashi Omori, Kandai Nozu, Kazumichi Fujioka, Naoto Takahashi, Tetsushi Yoshikawa, Hiroyuki Moriuchi, Yoshinori Ito, Akira Oka
- 掲載誌
- Journal of Clinical Medicine (2022,11(13),3582)