神戸大学大学院医学研究科の向山順子博士、藤田医科大学の下野洋平教授らの研究グループは、九州大学、Columbia大学との共同研究により、手術検体から分離した「がん幹細胞」を解析することで、マイクロRNA-221※1が大腸がんの「がん幹細胞」制御因子であること、およびその制御機構を解明しました。本成果により、今後、マイクロRNA-221の抑制による「がん幹細胞」を標的とした治療方法の開発が期待できます。
本研究成果は、2019年10月2日に、米国科学雑誌「Cancer Research」にオンライン掲載されました。
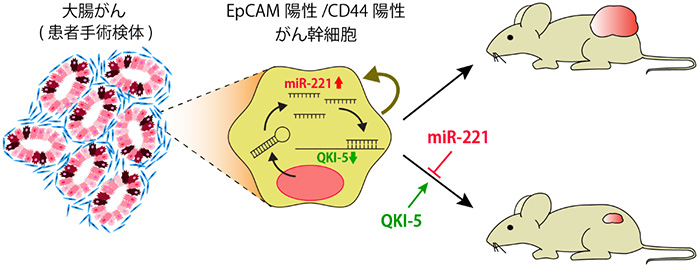
大腸がん幹細胞では癌に促進的に働く遺伝子であるマイクロRNA-221が選択的に上昇しており、RNA結合蛋白質QKI-5に結合し発現を抑制することで、腫瘍原性や幹細胞性の獲得に貢献する。
ポイント
- 大腸がん組織中の大腸がん幹細胞のマイクロRNAプロファイルを世界に先駆け解明
- 大腸がん幹細胞では、マイクロRNA-221の発現が選択的に上昇していることを発見
- マイクロRNA-221が大腸がんの幹細胞性を制御する機能をもつことを解明
- マイクロRNA-221の標的遺伝子としてRNA結合蛋白質QKI-5を同定
- マイクロRNA-221の抑制によるがん幹細胞を標的とした治療薬の開発に期待
研究の背景
がん幹細胞は「自己再生能と、腫瘍を構成するさまざまな系統のがん細胞を生み出す能力を持つ細胞」と定義される特殊な細胞集団です。がん幹細胞は高い腫瘍原性を持ち、化学療法や放射線療法などに対しても高い抵抗性を示すことで、がんの進展に重要な役割を果たすために、がん幹細胞を標的とした治療方法の開発が臨床的にも望まれています。
本研究グループはこれまでに、乳がん幹細胞の機能がマイクロRNAにより制御されていることを同定しました (Shimono Y et al. Cell 2009; Isobe T, Shimono Y et al. eLife 2014)。がん幹細胞は、大腸がんでもがんの発生、治療抵抗性、再発、転移などに重要な働きをすることが示されていますが (Dalerba P et al. PNAS 2007; Dalerba P, Shimono Y et al. Nature Biotechnology 2011; Mukohyama J, Shimono Y et al. Cancers 2017)、ヒト大腸がん幹細胞の制御にどのようなマイクロRNAが関わっているのかは明らかではありませんでした。そこで本研究グループは、手術で摘出した大腸がん組織から、薬品や凍結による修飾がなく生体内により近い状態のがん幹細胞を分離することで、マイクロRNAによる大腸がん幹細胞の制御機構を明らかにすることを目指しました。
研究の内容
本研究では、大腸がんの手術検体から分離したがん幹細胞を解析し、マイクロRNA-221が大腸がんの「がん幹細胞制御因子」であることを解明しました。
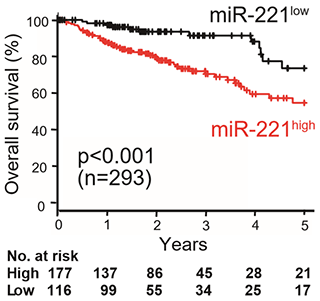
miRNA-221を高発現する大腸がん患者は、低発現の患者より生存率が低い。
まず、大腸がんの手術検体よりがん幹細胞を分離し、754種類のマイクロRNAの発現をスクリーニングしました。その結果、特にがん関連マイクロRNAとして注目されるマイクロRNA-221が、がん幹細胞で非常に高く発現していることが初めて明らかになりました。さらに、リアルタイムPCR法※2にて大腸がん幹細胞のマイクロRNA-221の発現レベルを測定したところ、通常の大腸がん細胞と比較し有意に高いことを明らかにしました。また、大規模がんゲノムデータベースのオミックス解析※3から、マイクロRNA-221が高発現している大腸がんの患者は、低発現の患者に比べ予後不良であることが分かりました (図1)。
次にヒト大腸がん細胞株とヒト大腸がん異種移植マウスの細胞を用いた3次元培養により、マイクロRNA-221の発現を抑制した大腸がん細胞では、腫瘍形成や増殖など、がん幹細胞のもつ基本的な機能が顕著に抑制されることを見出しました (図2A)。さらに、マウスへの移植実験によりマイクロRNA-221の発現抑制が大腸がんの腫瘍形成を顕著に抑えることを明らかにしました (図2B)。
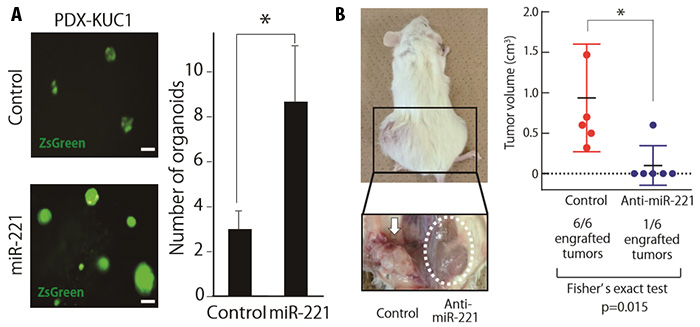
(A) miRNA-221の発現を増強すると大腸がん細胞の増殖能は増強する。
(B) miRNA-221の発現を抑制すると大腸がん細胞の腫瘍形成能は抑制される。
さらに、マイクロRNA-221の標的遺伝子としてRNA結合タンパク質QKI-5を見出し、マイクロRNA-221ががん幹細胞遺伝子として働く際には、QKI-5を抑制することが重要であることを明らかにしました。QKI-5の発現を増強すると、miR-221を抑制した時と同様に大腸がんのがん幹細胞のもつ基本的な機能は抑制されました (図3)。
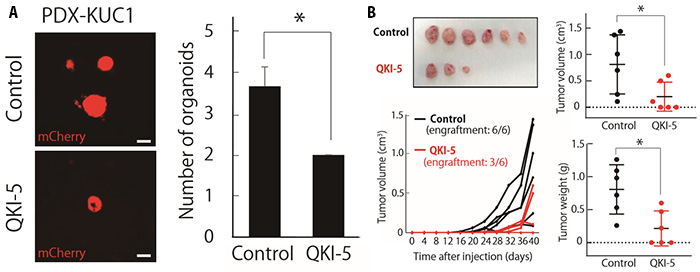
(A) QKI-5の発現を増強すると大腸がん細胞の増殖能は抑制される。
(B) QKI-5の発現を増強すると大腸がん細胞の腫瘍形成能は抑制される。
今後の展開
本研究により、がん関連マイクロRNAとして注目されるマイクロRNA-221が大腸がん幹細胞で特徴的に発現上昇しており、幹細胞性を制御することが明らかになりました。本研究グループは、乳がんのがん幹細胞でもマイクロRNA-221の発現上昇がみられることをすでに見出しており、マイクロRNA-221は大腸がんと乳がんに共通するがん幹細胞の制御因子であると考えられます。マイクロRNA-221を抑制する核酸創薬による治療法を見出すことで、将来的には大腸がんや乳がんに限らず多くのがん種の治療効果を高められるようになることが期待されます。
用語解説
- 1. マイクロRNA
- 標的遺伝子の3'末端に結合することでタンパク質への翻訳を抑制する22塩基程度の短い一本鎖RNA。一種類で数百の遺伝子の発現を抑制する能力をもち、幹細胞の性質の維持にも重要な働きをすることが示されてきています。
- 2. リアルタイムPCR法
- 特定の遺伝子断片を酵素反応で増幅しリアルタイムに検出することで、試料中の遺伝子発現量の定量を行う実験手法。
- 3. オミックス解析
- 生物の中にある分子全体の変動を探索し、生命現象を包括的に調べる解析手法。
謝辞
本研究は、文部科学省科学研究費補助金、高松宮妃癌研究基金研究助成、金沢大学がん進展制御研究所共同研究費、公益財団法人日本応用酵素協会研究助成、一般財団法人伊藤忠兵衛基金学術研究助成金、公益財団法人上原記念生命科学財団、公益財団法人細胞科学研究財団などの支援により行われました。
論文情報
- タイトル
- “miR-221 targets QKI to enhance the tumorigenic capacity of human colorectal cancer stem cells”
- DOI
- 10.1158/0008-5472.CAN-18-3544
- 著者
- Junko Mukohyama, Taichi Isobe, Qingjiang Hu, Takanori Hayashi, Takashi Watanabe, Masao Maeda, Hisano Yanagi, Xin Qian, Kimihiro Yamashita, Hironobu Minami, Koshi Mimori, Debashis Sahoo, Yoshihiro Kakeji, Akira Suzuki, Piero Dalerba and Yohei Shimono
- 掲載誌
- Cancer Research