神戸大学大学院医学研究科の仁田亮教授、博士課程大学院生の田口真也氏、今崎剛助教らの研究グループは、理化学研究所放射光科学研究センター生物系ビームライン基盤グループの坂井直樹研究員 (研究当時、現高輝度光科学研究センター構造生物学推進室研究員)、同重松秀樹研究員 (研究当時、現高輝度光科学研究センター構造生物学推進室研究員)、東北大学大学院生命科学研究科修士課程大学院生の中野朱莉氏、東北大学学際科学フロンティア研究所の丹羽伸介准教授らとの共同研究により、分子モーターキネシンが細胞骨格である微小管※1の伸長速度をコントロールして、神経細胞などの突起の長さを調節するしくみをX線結晶構造解析※2や全反射照明蛍光顕微鏡※3を用いて明らかにしました。本研究成果は、神経細胞、上皮細胞などの細胞を形づくる際に用いられる、細胞の根源的なしくみを説明するものです。
この研究成果は、2022年9月6日に、国際学術雑誌「eLife」にオンライン掲載されました。
ポイント
- X線結晶構造解析法を用いて、微小管の構成蛋白質チューブリンとキネシンの一つであるKLP-12の相互作用を原子分解能で明らかにした。
- KLP-12が微小管伸長速度を緩めるブレーキの役割を果たすことをTIRF顕微鏡により明らかにした。
研究の背景
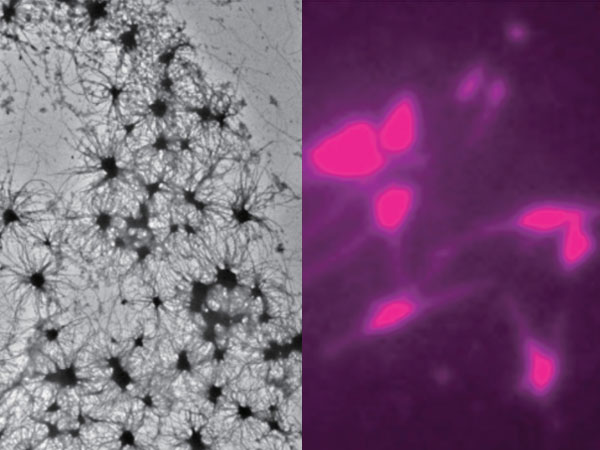
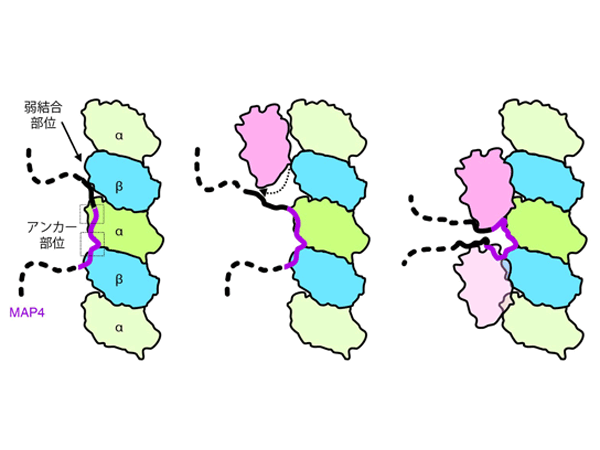
細胞は、上皮細胞の繊毛や神経細胞の軸索など、様々な種類の突起を形成し、細胞種に応じた機能を発揮しています。突起の長さは、突起の軸に沿って伸長する最も太い細胞骨格分子である微小管の長さにより規定されます。微小管は伸びたり縮んだりを繰り返す性質をもち、伸びる時 (重合*4) と縮む時 (脱重合*4) とでは微小管のプラス端側の外側への反り返りの度合いが違います。微小管末端がまっすぐであれば微小管の重合に、端が反り返っていれば微小管の脱重合が誘導されます。この湾曲は多くの因子によって制御されており、微小管モーターキネシンの一つであるKLP-12もその一つです。神経細胞の発達、疾患との関連からも重要な仕組みですが、この制御の分子機構の詳細は未解明です。
研究の内容
KLP-12はkinesin-4 ファミリーに属する線虫のキネシンで、kinesin-4ファミリーのキネシンが微小管のダイナミクスを制御する現象については様々な報告がされていますが、キネシンが微小管の末端でどのように振る舞い、微小管のダイナミクスを制御しているのかはほとんどわかっていませんでした。そこで我々は、線虫の遺伝学的解析、生化学、全反射照明蛍光 (TIRF) 顕微鏡、大型放射光施設SPring-8の高輝度X線を用いたX線結晶構造解析を駆使してこの疑問に答えました。
まず、KLP-12変異体の線虫の遺伝学的スクリーニングを行いました。その結果KLP-12のエクソン4-6を欠失しフレームシフトを持つ変異体や末端ドメイン欠失変異体では、ALM*5、PLM*6ニューロンの軸索突起が異常に伸長することがわかりました。そこで、KLP-12を組換えタンパク質発現系で発現・精製し、KLP-12が微小管伸長に及ぼす影響をTIRF顕微鏡で観察しました。KLP-12存在下で微小管伸長速度を観察したところ、KLP-12の濃度が高くなるほど微小管の伸長がゆっくりになることが明らかとなりました。またKLP-12の動きをよく見ると、微小管プラス端方向に移動し、末端まで行くとそのまま末端には留まらず、脱落していく事が分かりました。面白いことに、伸長速度は抑制されますが、微小管の縮む速度や崩壊の頻度には大きな差は見られませんでした。
次に研究グループはKLP-12が微小管伸長速度をどのように調節しているのかを明らかにするため、X線結晶構造解析を行いました。KLP-12が微小管の末端 (プラス端) に結合した状態を模すため、微小管のプラス端に結合する人工タンパク質DARPinを、遺伝子クローニングでKLP-12 C末端に導入し、微小管が重合しない工夫を施しました。微小管の構成蛋白質であるチューブリンとKLP-12-Darpinをゲル濾過クロマトグラフィーで精製し、結晶化を行ったところ、良質な結晶を得ることに成功しました。この結晶を兵庫県にある大型放射光施設SPring-8のビームラインBL32XUの微小集光X線を用いてデータ測定を行い解析した結果、チューブリン-KLP-12-DARPin複合体の構造を2.9Å (オングストローム) 分解能で明らかにすることに成功しました。
構造解析の結果、KLP-12は通常のキネシンと同様にチューブリン二量体の間に結合していました。結晶化の際に入れたATPアナログの電子密度もしっかりと確認出来たことから、ATP結合型を取っていることが分かりました。次にKLP-12の構造を、微小管重合を誘導するKIF5Bキネシン、脱重合を誘導するKIF2Cキネシンと比較しました。するとKLP-12は、KIF5Bと非常に類似した構造を取りながら、チューブリンに面する一部側鎖の相互作用の強さから、チューブリン二量体をキネシン側 (微小管の外側) に3度ほど曲げていることが分かりました。KIF2Cと比較してみたところ、KIF2CはKLP-12には存在しないループを持っており、KLP-12よりさらに3度ほど大きくチューブリン二量体を曲げていることが分かりました。これらのことからKLP-12は重合誘導型のKIF5Bと脱重合誘導型のKIF2Cの中間にチューブリンの曲率を保つことにより、微小管伸長速度を緩めていることが明らかとなりました。
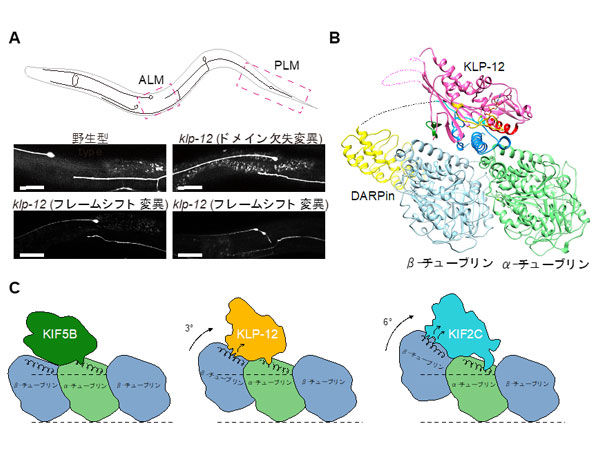
A. KLP-12 による線虫ALM、PLMニューロン伸長制御。模式図 (上) と野生型、変異体 (klp-12) の表現系。ALMニューロンとPLMニューロンの過剰伸長が観察される。
B. チューブリン-KLP-12-DARPin 4者複合体のX線結晶構造。α-チューブリンを緑、β-チューブリンをシアン、DAPRinを黄色、KLP-12をマジェンタで表示。
C. KLP-12による微小管末端制御機構の模式図。微小管伸長を催すKIF5Bを左、微小管伸長速度を遅くするKLP-12を真ん中、微小管の脱重合を催すKIF2Cを右に示す。
今後の展開
本研究は、kinesin-4モータードメインによる微小管ダイナミクスの制御機構を原子レベルで明らかにしました。軸索の形態形成、シナプス形成、微小管ネットワーク構築のメカニズムの理解がさらに進むと思われます。また、様々な神経変性疾患の原因となるKLP-12のオルソログであるKIF21A/Bの機能障害による疾患発症の分子機構を解明し、新たな治療戦略を開発するための出発点となります。
用語解説
- ※1 微小管
- 細胞内で最大の細胞骨格分子。α、β-チューブリン二量体が縦に連なったプロトフィラメントが13本並び、中空管状の構造をしている。
- ※2 X線結晶構造解析
- X線を用いて結晶の原子構造を決定する手法。今回の場合はタンパク質を結晶化し、複数の結晶から大型放射光施設SPring-8 BL32XU の高輝度微小X線を用いてデータ収集を行い、それらを統合し解析を行った。
- ※3 全反射照明蛍光顕微鏡
- トンネル効果によりしみ出すレバネッセント光を励起光源とした蛍光顕微鏡です。光学顕微鏡より高い分解能を備えるため、微小管や微小管結合タンパク質一分子の観察が可能である。
- ※4 重合、脱重合
- 微小管がGTPチューブリンを取り込み伸長することを重合、チューブリンがGDP型となった後に脱離し微小管が退縮していくことを脱重合と言う。
- ※5 ALMニューロン
- Anterior Lateral Mechanosensory ニューロン。機械的刺激を感知し、鼻から体中央部にかけての触覚に反応する。
- ※6 PLMニューロン
- Posterior Lateral Mechanosensory ニューロン。機械的刺激を感知し、体中央部から尾にかけての触覚に反応する。
謝辞
本研究は、文部科学省科研費学術変革領域研究A「クロススケール細胞内分子構造動態解析が解明する細胞骨格ネットワーク構築とその破綻 (クロススケール新生物学)」(研究代表者: 仁田亮)、「軸索輸送モーターKIF5Aによる長距離輸送機構と疾患のクロススケール解析 (クロススケール新生物学)」 (研究代表者:丹羽伸介)、内閣府ムーンショット型研究開発事業「臓器連関の包括的理解に基づく認知症関連疾患の克服に向けて」(研究代表者: 高橋良輔)、日本医療研究開発機構 (AMED) 革新的先端研究開発支援事業ユニットタイプ (AMED-CREST)「心筋メカノバイオロジー機構の解明による心不全治療法の開発 (メカノバイオロジー機構の解明による革新的医療機器及び医療技術の創出)」(研究代表者:小室一成)、科学技術振興機構 (JST) 創発的研究支援事業「微小管を軸とした細胞極性形成機構の解明」(研究代表者:今崎剛)、「革新的化合物探索・合成手法による新規抗菌アジュバントの創出 (感染症創薬に向けた研究基盤の構築と新規モダリティ等の技術基盤の創出)」(研究代表者:鈴木仁人)、文部科学省科研費、武田科学振興財団、持田記念医学薬学振興財団、上原生命科学財団等の支援を受けて行ったものです。
論文情報
- タイトル
- “Structural model of microtubule dynamics inhibition by kinesin-4 from the crystal structure of KLP-12 –tubulin complex”
- DOI
- 10.7554/eLife.77877
- 著者
- Shinya Taguchi1,2†, Juri Nakano3†, Tsuyoshi Imasaki1†, Tomoki Kita4, Yumiko Saijo-Hamano1, Naoki Sakai5, Hideki Shigematsu5, Hiromichi Okuma1, Takahiro Shimizu1, Eriko Nitta1, Satoshi Kikkawa1, Satoshi Mizobuchi2, Shinsuke Niwa3,4,6*, Ryo Nitta1*
1 Division of Structural Medicine and Anatomy, Department of Physiology and Cell Biology, Kobe University Graduate School of Medicine
2 Division of Anesthesiology, Kobe University Graduate School of Medicine
3 Graduate School of Life Sciences, Tohoku University
4 Department of Biology, Faculty of Science, Tohoku University
5 RIKEN SPring-8 Center
6 Frontier Research Institute for Interdisciplinary Sciences (FRIS), Tohoku University
† These authors contributed equally to this work
* corresponding authors - 掲載誌
- eLife