神戸大学大学院医学研究科 附属感染症センター臨床ウイルス学分野 森康子教授らの研究グループは、ヒトヘルペスウイルス6B(HHV-6B)感染症に対するワクチンの開発を目指し、HHV-6Bの糖タンパク質複合体gH/gL/gQ1/gQ2のワクチンとしての有効性を明らかにしました。HHV-6B感染症に対しては未だ治療法及び予防法がなく、本研究は世界でも初となるワクチン開発の試みです。
本研究は、神戸大学大学院医学研究科生化学・分子生物学講座シグナル統合学分野 的崎尚教授ら、同病理学講座病理診断学分野 伊藤智雄教授ら、同内科系講座皮膚科学分野 錦織千佳子教授、大阪大学微生物病研究所BIKEN次世代ワクチン協働研究所ワクチン動態プロジェクト 青枝大貴准教授ら、帝京大学薬学部薬物送達学研究室 鈴木亮教授ら、並びに一般財団法人阪大微生物病研究会との共同研究によって実施されました。
この研究成果は、7月23日付けで米国科学雑誌「PLOS Pathogens」にオンライン掲載されました。
ポイント
- ヒトヘルペスウイルス6B(HHV-6B)は、ほぼ全てのヒトが乳幼児期に感染する病原体で、発熱を伴う突発性発疹※1の原因となるだけでなく、熱性痙攣や脳炎・脳症と言った後遺症の残る重篤な合併症を引き起こす事が知られている。
- HHV-6B感染症に対する有効な治療法・予防法は未だ確立されておらず、極めて高い感染率や潜在的リスクの高さから、ワクチンが開発される事で小児の予防接種を実現し、広く予防する事が望まれている。
- 本研究では、同研究グループが発見したHHV-6B感染の鍵となるウイルスの糖タンパク質複合体をワクチン抗原として応用し、その有効性を解析した。
- 精製したウイルス抗原を免疫賦活化剤※2と共にマウスに接種する事で、HHV-6Bに対する効果的な免疫が誘導できることが実証でき、また免疫賦活化剤の組み合わせによって、細胞性免疫※3も誘導できる事が示された。
- HHV-6B感染症に対する安全で有効なワクチンの実現に向けた大きな足掛かりとなる成果であり、今後臨床試験へと進めていく事が期待される。
研究の背景
ヒトヘルペスウイルス6(HHV-6B)は、家族などから唾液を通じて乳幼児に感染し、38℃以上の発熱と全身の発疹を呈する突発性発疹の原因となります。HHV-6Bはほぼ全ての人が感染しています。その感染時期は生後6ヵ月から2歳であると知られていて、母親から受け継いだ移行抗体が減衰していく時期と一致しています。多くの場合、小児のHHV-6B感染症は深刻な症状には至らず治癒しますが、時として重篤な合併症に繋がってしまうことがあり、日本でも年間150人ほどの小児が脳炎・脳症を発症して、その半数で後遺症が残る事が報告されています。しかしHHV-6Bに対して効果的な治療法・予防法は確立されておらず、乳幼児とその家族の暮らしをHHV-6B感染症から守るためにはワクチンの開発が必要不可欠です。
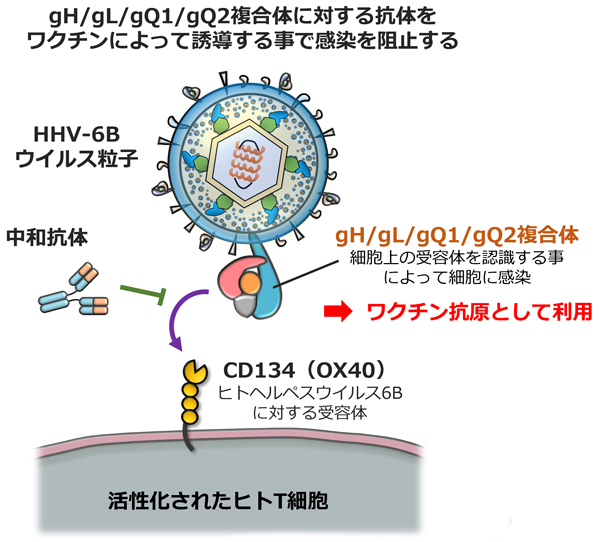
森康子教授の研究グループはこれまでの研究で、HHV-6Bのウイルス表面に発現する糖タンパク質複合体gH/gL/gQ1/gQ2を発見し、その複合体が活性化したT細胞上のCD134(OX40)を認識する事が感染の鍵であることを発見してきました(図1)。このgH/gL/gQ1/gQ2複合体に対する抗体はHHV-6Bの感染を阻止できる事から、マウスで得られた抗体を基にヒトで利用可能なヒト化抗体を作製するといった研究も進めています。これらの知見から、gH/gL/gQ1/gQ2複合体を体内に接種する事で、この複合体に対する免疫を誘導できれば、HHV-6Bの感染に有効な免疫の獲得に繋がるという着想に至りました。
研究の内容
本研究ではHHV-6B gH/gL/gQ1/gQ2複合体を基としたワクチン開発を行いました(特許出願 2017-509816 特許査定済み 一般財団法人阪大微生物病研究会及び国立大学法人神戸大学)。遺伝子組換え技術によってgH/gL/gQ1/gQ2複合体を作製し、ワクチン抗原として免疫賦活化剤と共にマウスに接種する事でその免疫誘導能を解析しました(図2)。
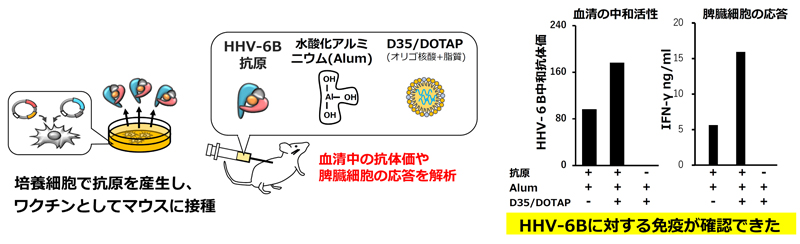
HHV-6B gH/gL/gQ1/gQ2複合体は、四種類のタンパク質が細胞内で組み立てられる複雑な分子であるため、培養細胞内でそれらを同時に発現させる系を確立しました。この発現系から得られたgH/gL/gQ1/gQ2複合体は標的細胞の受容体分子であるCD134(OX40)に対して結合し、その機能が保持されている事が示されました。
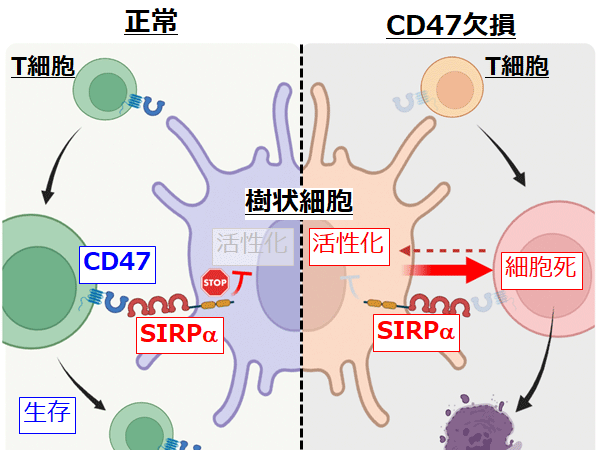
gH/gL/gQ1/gQ2複合体を、現行のワクチンで広く使用されている免疫賦活化剤の水酸化アルミニウムと混合してマウスへ複数回接種し、免疫応答を解析しました。その結果、マウスの血清中にgH/gL/gQ1/gQ2複合体に対する抗体が誘導される事が確認でき、それらの血清は実際にHHV-6Bの細胞への感染を阻害することが示されました。またこの糖タンパク複合体自体が樹状細胞を活性化する事が示され、自然免疫※4を誘導する性質がある事も示唆されました。
水酸化アルミニウムに加えて、免疫賦活化剤として細胞性免疫の誘導能があるオリゴ核酸D35とその送達を補助する脂質DOTAPを混合した物質を添加したワクチンでは、より強い抗体誘導が確認できました。免疫実験を行ったマウスの脾臓から脾臓細胞を抽出して、ワクチン抗原であるgH/gL/gQ1/gQ2複合体に対する免疫細胞の応答を調べた結果、D35/DOTAPを添加した群でより強い応答が見られ、細胞性免疫の誘導が確認できました。さらなる解析の結果、主に応答しているのはCD4陽性T細胞である事が示されました。
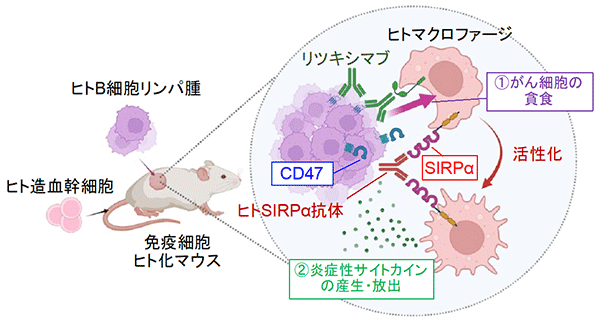
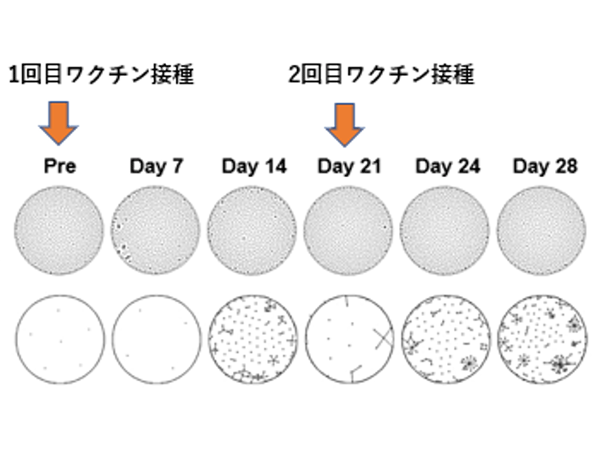
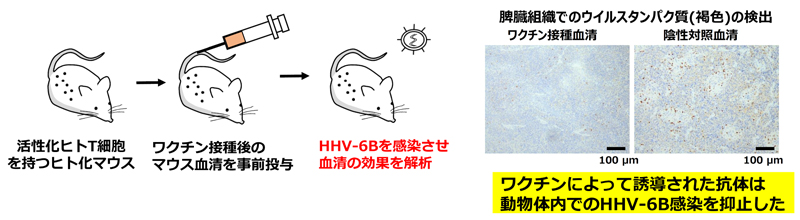
HHV-6B gH/gL/gQ1/gQ2複合体の接種により誘導された血清中の抗体が、動物体内で実際にHHV-6B感染を阻止できるかどうかについても検証を行いました(図3)。この実験では免疫細胞ヒト化マウス※5の利用によるHHV-6B感染病態動物モデルが用いられました。陰性対照としてgH/gL/gQ1/gQ2複合体を含まない免疫賦活化剤のみのワクチンを接種したマウスの血清を事前に投与したヒト化マウスでは、HHV-6Bの接種によってマウス体内でウイルスが増殖し、脾臓で多くのウイルス抗原が検出されました。一方でgH/gL/gQ1/gQ2複合体を含むワクチンを接種したマウスから得られた血清を事前投与したヒト化マウスでは、ウイルスが増加せず、脾臓でのウイルス抗原もほとんど見られなかったことから、ワクチンにより誘導された免疫が動物体内で起こるHHV-6B感染に対しても有効である事が示されました。
今後の展開
全ての乳幼児の健康を脅かし得る潜在的な危険性にも関わらず、HHV-6B感染症に対しては未だに有効な治療法・予防法が確立されていません。本研究で得られた成果はHHV-6B感染症に対するワクチンでの予防を実現する第一歩となるものです。gH/gL/gQ1/gQ2複合体を抗原とした今回のワクチンは効率的に免疫を誘導する事が示され、また他のウイルス由来分子を含まないサブユニットワクチン※6であるため、安全性にも期待が持たれます。現在、生後3か月の乳幼児に定期接種されている四種混合ワクチン(ジフテリア、百日せき、破傷風、ポリオ)と同時期の接種、あるいは本ワクチンを加えた五種混合ワクチンとして接種する事で、乳幼児をHHV-6B感染から予防する事が可能であると考えています。
HHV-6Bは感染後、生涯に渡って体内に潜伏感染する性質を持ち、薬物過敏症症候群や免疫力の低下などに伴って体内で再活性化する事で、様々な疾病を引きこす事が報告されています。特に白血病などの治療として造血幹細胞移植を行った際には高頻度でHHV-6Bの再活性化が起こり、致死性の脳炎を引き起こす事が問題となっています。本研究のワクチンは免疫賦活化剤の組み合わせによって、抗体を産生する液性免疫※7だけではなく、細胞性免疫も誘導できる事が示されたため、HHV-6B感染に対するより強力な免疫を誘導する事も可能であり、造血幹細胞移植時のHHV-6B感染症の抑制にも応用が可能であると考えられます。
今後、本研究で得られた成果を基に、さらにワクチンの有効性および安全性のデータを集積し、臨床試験へ繋げていく事で、世界に先駆けて日本発のHHV-6Bワクチンを実現させるための研究を継続していきます。
用語解説
※1 突発性発疹
生後6ヵ月ごろから乳幼児が罹患する病気で、発熱と解熱後の発疹が特徴です。主にHHV-6Bの感染が原因で、他にも類縁のヘルペスウイルスであるヒトヘルペスウイルス7(HHV-7)の感染によっても引き起こされる事があります。通常は予後良好ですが、まれに熱性痙攣や脳炎・脳症といった重篤な合併症を起こす事が問題となっています。
※2 免疫賦活化剤
アジュバントとも呼ばれ、体内の免疫機能を増強させる働きがあります。ワクチンにおいては抗原と併せて用いることで、抗原への免疫反応を増強し、より効果的な免疫の獲得を促します。
※3 細胞性免疫
外来の抗原を特異的に認識したT細胞が、マクロファージや細胞傷害性T細胞を活性化させる事で標的となる病原体などを排除する免疫機構です。
※4 自然免疫
外来の病原体などの異物に対して免疫細胞が広く反応する事で、免疫機能が活性化される機構です。
※5 免疫細胞ヒト化マウス
免疫細胞が欠損しているマウスにヒト造血幹細胞を移植する事で、ヒトの免疫細胞を保有するマウス(ヒト化マウス)としたものです。HHV-6BはヒトT細胞に特異的に感染するため、通常のマウスに接種しても感染は成立しませんが、HHV-6B感染病態動物モデルでは、ヒト化マウス体内でのHHV-6Bの感染と増殖が確認されています。
※6 サブユニットワクチン
病原体の一部分のみを用いたワクチンで、病原体表面で突出して感染に関わっている分子のような適切な抗原を選択する事で、効率的に有効な免疫を誘導させることができ、また接種に伴う副作用も低く抑える事ができると考えられています。弱毒病原体を使用する生ワクチンなどと比べて免疫誘導能が弱いため、免疫賦活化剤の効果的な利用が課題となります。
※7 液性免疫
外来の抗原を特異的に認識したT細胞がB細胞の抗体産生を促し、血液やリンパ液などに分泌された抗体が標的となる病原体などに結合する事で中和や排除に働く免疫機構です。
謝辞
本研究は一部、国立研究開発法人日本医療研究開発機構(AMED)医療分野研究成果展開事業産学連携医療イノベーション創出プログラム・セットアップスキーム(ACT-MS)「小児において疾病負荷が高い突発性発疹ウイルス感染症に対する新規ワクチン開発」(研究代表者:森康子)、厚生労働科学研究費補助金 厚生科学基盤研究分野 創薬基盤推進研究「ワクチン基礎生産技術の向上に関する研究」(研究代表者:森康子)及び疾病・障害対策研究分野 新型インフルエンザ等新興・再興感染症研究「利便性の高い五種混合ワクチンの開発に向けた研究」(研究代表者:森康子)、日本学術振興会 特別研究員奨励費(王博超)の支援を受けて実施されました。
論文情報
タイトル
DOI
10.1371/journal.ppat.1008609
著者
Bochao Wang1, Kouichi Hara1, Akiko Kawabata1, Mitsuhiro Nishimura1, Aika Wakata1, Lidya Handayani Tjan1, Anna Lystia Poetranto1, Chisato Yamamoto1, Yasunari Haseda2, Taiki Aoshi2,3, Lisa Munakata4, Ryo Suzuki4, Masato Komatsu5, Ryuko Tsukamoto5, Tomoo Itoh5, Chikako Nishigori6, Yasuyuki Saito7, Takashi Matozaki7, Yasuko Mori1
1 神戸大学大学院医学研究科附属感染症センター臨床ウイルス学分野
2 大阪大学微生物病研究所BIKEN次世代ワクチン協働研究所ワクチン動態プロジェクト
3 一般財団法人 阪大微生物病研究会BIKEN次世代ワクチン開発研究センター
4 帝京大学薬学部薬物送達学研究室
5 神戸大学医学部附属病院病理部
6 神戸大学大学院医学研究科内科系講座皮膚科学分野
7 神戸大学大学院医学研究科生化学・分子生物学講座シグナル統合学分野掲載誌